
Wetenschap
Beschrijf als een reeks stappen hoe tafelzout in water oplossing maakt die elektriciteit kan leiden?
1. Zout oplossen:
* ionische verbindingen: Tafelzout is een ionische verbinding, wat betekent dat deze wordt gevormd door de elektrostatische aantrekkingskracht tussen positief geladen natriumionen (Na+) en negatief geladen chloride-ionen (Cl-).
* Water als oplosmiddel: Water is een polair oplosmiddel, wat betekent dat de moleculen een enigszins positief uiteinde hebben en een enigszins negatief uiteinde. Met deze polariteit kunnen watermoleculen de geladen ionen in zout omringen en aantrekken.
* dissociatie: De watermoleculen trekken de Na+ en Cliions uit elkaar en breken de ionische bindingen die ze bij elkaar hielden in het zoutkristal. Deze ionen zijn nu vrij om in het water te bewegen.
2. Een geleidende route creëren:
* Mobiele ladingsdragers: De opgeloste Na+ en Clers in het water worden mobiele ladingsdragers. Ze kunnen vrij door de oplossing bewegen.
* elektrische stroom: Wanneer een elektrische potentiaal (een spanning) over de zoutoplossing wordt toegepast, reageren de ionen:
* Positieve Na+ -ionen bewegen naar de negatieve elektrode (kathode).
* Negatieve climes bewegen naar de positieve elektrode (anode).
* ladingsstroom: Deze beweging van ionen vormt een elektrische stroom. De oplossing is nu in staat om elektriciteit te leiden.
Samenvattend:
* Het oplossen van zout in water creëert vrij bewegende ionen.
* Deze ionen fungeren als ladingsdragers, waardoor de stroom van elektriciteit mogelijk is wanneer een spanning wordt toegepast.
Belangrijke opmerking: Zuiver water zelf is een zeer slechte geleider van elektriciteit. Het is de aanwezigheid van opgeloste ionen (zoals die uit zout) die de oplossing geleidelijk maken.
 Hoe noem je de vrijgegeven warmte wanneer 1 mol van een stof volledige verbranding ondergaat?
Hoe noem je de vrijgegeven warmte wanneer 1 mol van een stof volledige verbranding ondergaat?  Boornitride en zilveren nanodeeltjes om de uitstoot van koolmonoxide te verminderen
Boornitride en zilveren nanodeeltjes om de uitstoot van koolmonoxide te verminderen Lachgas:waarom het milieu niet blij is met lachgas
Lachgas:waarom het milieu niet blij is met lachgas  Waarom is ethanol minder zuur dan fenol?
Waarom is ethanol minder zuur dan fenol?  Waarom is benzoëzuur enigszins oplosbaar in water?
Waarom is benzoëzuur enigszins oplosbaar in water?
 Voor 's werelds meest illegaal verhandelde dier, een onwaarschijnlijke held
Voor 's werelds meest illegaal verhandelde dier, een onwaarschijnlijke held  Wetenschappers missen essentiële kennis over snelle Arctische klimaatverandering
Wetenschappers missen essentiële kennis over snelle Arctische klimaatverandering Hoe lang is 's werelds hoogste levende boom?
Hoe lang is 's werelds hoogste levende boom?  Olieopruiming begint nadat vrachtschepen bij Corsica in aanvaring komen
Olieopruiming begint nadat vrachtschepen bij Corsica in aanvaring komen Meteoriet bevat het oudste materiaal op aarde:7 miljard jaar oud sterrenstof
Meteoriet bevat het oudste materiaal op aarde:7 miljard jaar oud sterrenstof
Hoofdlijnen
- Begrijpen hoe een cel een persoon wordt, met wiskunde
- Wat is een wetenschapper die alles bestudeert?
- Hoe balsemen werkt
- De vijf belangrijkste redenen van een expert waarom honden als uitzonderlijke dieren kunnen worden beschouwd
- Onthoud mij? Geslacht en ras kunnen ervoor zorgen dat u vergeetbaar wordt
- Wat is het kleinste levende ding in de volgende lijst met kikkerembryo mitochondria bacteriënvirus atoom?
- Peervormige larve gevonden in weekdieren worden genoemd?
- Wat is de rol van proteolytische enzymen in de celcyclus?
- Wat veroorzaakt het bestaan?
- Een sleutel tot calciumsignalering:structuur van de menselijke IP3R type 3 in zijn ligandvrije toestand

- Ga de piste op met biobased ski's en snowboards

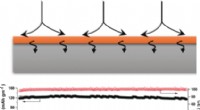
- Hybride indium-lithiumanoden zorgen voor snel grensvlak-ionentransport
- Onderzoekers ontwikkelen hulpmiddel om te helpen bij ontwikkeling, efficiëntie van auto's op waterstof

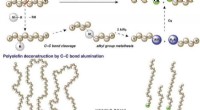
- Kunststoffen kunnen een tweede leven krijgen als biologisch afbreekbare oppervlakteactieve stoffen
 Beweging van water en vallende rotsen zijn een voorbeeld van welke energie?
Beweging van water en vallende rotsen zijn een voorbeeld van welke energie?  Waarom is zwaveldioxide polair en koolstof non wanneer beide covalente binding hebben?
Waarom is zwaveldioxide polair en koolstof non wanneer beide covalente binding hebben?  Hoe beïnvloedt licht het ecosysteem?
Hoe beïnvloedt licht het ecosysteem?  Californië wildvuur ontploft, brandend over 25 mijl in dag
Californië wildvuur ontploft, brandend over 25 mijl in dag Wat zijn de sub-branches van astrofysica?
Wat zijn de sub-branches van astrofysica?  Waarom Neptunus soms verder van de zon dan Pluto?
Waarom Neptunus soms verder van de zon dan Pluto?  Wat is een niet-voorbeeld van lysosoom?
Wat is een niet-voorbeeld van lysosoom?  Hoe de grootste gemeenschappelijke factor van twee nummers te vinden
Hoe de grootste gemeenschappelijke factor van twee nummers te vinden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

