
Wetenschap
Welke alle metalen hebben lage smelt- en kookpunten?
metalen met lage smeltpunten:
* Mercury (Hg): De enige metalen vloeistof bij kamertemperatuur (smeltpunt -38,83 ° C).
* Gallium (GA): Smelt net boven kamertemperatuur (smeltpunt 29,76 ° C). Het wordt vaak gebruikt in thermometers op hoge temperatuur.
* cesium (CS): Het laagste smeltpunt van alle metalen (smeltpunt 28,44 ° C). Het is erg reactief en moet met zorg worden behandeld.
* Francium (FR): Een radioactief metaal met een smeltpunt dat wordt geschat op ongeveer 27 ° C, waardoor het erg moeilijk is om te bestuderen.
* rubidium (RB): Smelt bij 39.31 ° C.
metalen met lage kookpunten:
* Mercury (Hg): Heeft ook een relatief laag kookpunt (356,73 ° C).
* cesium (CS): Kookt op 671 ° C, waardoor het een van de meest vluchtige metalen is.
* rubidium (RB): Kookt op 688 ° C.
* Francium (FR): Heeft waarschijnlijk een laag kookpunt, maar het is moeilijk te meten vanwege zijn radioactiviteit.
* kalium (k): Kookt bij 759 ° C.
* natrium (NA): Kookt op 883 ° C.
Waarom hebben sommige metalen een laag smelten- en kookpunten?
* Zwakke metalen binding: Metalen met lage smelt- en kookpunten hebben relatief zwakke metalen bindingen. Deze bindingen worden gevormd door het delen van elektronen in een "zee" van gedelokaliseerde elektronen. Hoe zwakker de binding, hoe minder energie nodig is om het te breken, wat leidt tot lagere smelt- en kookpunten.
* Atomaire grootte en elektronenconfiguratie: Grotere atomen met meer losjes gehouden elektronen hebben een zwakkere metalen binding. Dit is de reden waarom alkali -metalen (zoals lithium, natrium, kalium) de neiging hebben om lage smelt- en kookpunten te hebben.
* Elektronenconfiguratie: Het aantal valentie -elektronen (elektronen in de buitenste schaal) beïnvloedt ook de metaalbindingssterkte. Metalen met minder valentie -elektronen hebben over het algemeen zwakkere bindingen.
Belangrijke opmerking: De reactiviteit van sommige van deze metalen (vooral alkali -metalen) maakt ze een uitdaging om mee te werken. Ze moeten in inerte atmosferen worden behandeld om reacties met lucht en vocht te voorkomen.
 Wat is de pH van zoutzuur wanneer gemengd met magnesiumcarbonaat?
Wat is de pH van zoutzuur wanneer gemengd met magnesiumcarbonaat?  H2O CO2 C12HO Zijn voorbeelden van wat?
H2O CO2 C12HO Zijn voorbeelden van wat?  Wat zegt hoogwaardig onderzoek over de milieueffecten van radiogolven?
Wat zegt hoogwaardig onderzoek over de milieueffecten van radiogolven?  Kegelvormig gereedschap dat u helpt vloeistoffen of fijne poeders in een smalle opening te gieten zonder te morsen?
Kegelvormig gereedschap dat u helpt vloeistoffen of fijne poeders in een smalle opening te gieten zonder te morsen?  Een nieuw recept voor luchtstabiel en hoogkristallijn radicaal-gebaseerd coördinatiepolymeer
Een nieuw recept voor luchtstabiel en hoogkristallijn radicaal-gebaseerd coördinatiepolymeer
 Wie zei dat je met diepgaand respect de oneindige capaciteit van de menselijke geest moet bekijken om de nuttige kennis van de mens te weerstaan?
Wie zei dat je met diepgaand respect de oneindige capaciteit van de menselijke geest moet bekijken om de nuttige kennis van de mens te weerstaan?  El Nino voedde de Zika-uitbraak, nieuwe studie suggereert:
El Nino voedde de Zika-uitbraak, nieuwe studie suggereert: Dodelijke hittegolven zullen blijven stijgen, studie vondsten
Dodelijke hittegolven zullen blijven stijgen, studie vondsten Bewolkte klimaatvoorspellingen opruimen
Bewolkte klimaatvoorspellingen opruimen Nieuw rapport schetst mogelijke opbrengstuitdagingen voor opschaling van natuurlijke landbouw zonder budget in India
Nieuw rapport schetst mogelijke opbrengstuitdagingen voor opschaling van natuurlijke landbouw zonder budget in India
Hoofdlijnen
- Welke planeet heeft levende organismen?
- Studie koppelt koudwaterschok aan catastrofale instorting van koraal in de oostelijke Stille Oceaan
- Een bepaalde diersoort heeft zes paren chromosomen Hoeveel DNA -moleculen zijn deze dieren tijdens de G2 -fase aanwezig in de kernen?
- Hoeveel wetenschapsvelden zijn er?
- Wat is een verklaring op basis van veel observaties en ondersteund door de resultaten van experimenten?
- Welke objecten zetten zonlicht om in suikers?
- Wat is in de fysieke wetenschap niet wat is het verschil tussen een gesloten systeem en een open systeem?
- Wat testen wetenschappers?
- Dieetgeheimen van 'the Royals' - Isotopen van haar van olifantenstaarten laten zien dat vee de dikhuiden verslindt
- Meringue-achtig materiaal kan vliegtuigen zo stil maken als een haardroger

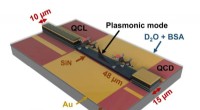
- Geminiaturiseerde lab-on-a-chip voor realtime chemische analyse van vloeistoffen
- Een sleuteldeel van de cel decoderen, atoom voor atoom

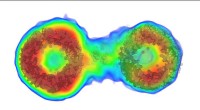
- Krachtige nieuwe beeldvormingsmethode onthult in detail hoe deeltjes in oplossing bewegen
- Onderzoekers ontwerpen een verbeterde route naar koolstofneutrale kunststoffen

 Seizoensgebonden moessonregens blokkeren de belangrijkste oceaanstroming
Seizoensgebonden moessonregens blokkeren de belangrijkste oceaanstroming Cyprus:klimaatverandering, achteruitgang op het platteland verhoogt het risico op bosbranden
Cyprus:klimaatverandering, achteruitgang op het platteland verhoogt het risico op bosbranden Toezicht op schoolhoofden moet gericht zijn op instructief leiderschap, volgens onderzoek
Toezicht op schoolhoofden moet gericht zijn op instructief leiderschap, volgens onderzoek Nanodeeltjes en Mini-NMR wijzen de weg naar gepersonaliseerde kankertherapie
Nanodeeltjes en Mini-NMR wijzen de weg naar gepersonaliseerde kankertherapie Hoe magneten werken
Hoe magneten werken  Het terugwinnen van drugs uit riolen kan de schade aan dieren in het wild verminderen
Het terugwinnen van drugs uit riolen kan de schade aan dieren in het wild verminderen Qantas houdt vliegtuigen aan de grond, CEO ziet af van loon naarmate het virus zich verspreidt
Qantas houdt vliegtuigen aan de grond, CEO ziet af van loon naarmate het virus zich verspreidt Wat is het verschil tussen antebrachium en brachium?
Wat is het verschil tussen antebrachium en brachium?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

