
Wetenschap
Wat is de pH van zoutzuur wanneer gemengd met magnesiumcarbonaat?
De reactie
Hydrochloorzuur (HCL) is een sterk zuur, terwijl magnesiumcarbonaat (MGCO3) een basis is. Wanneer ze reageren, ondergaan ze een neutralisatiereactie en produceren ze:
* magnesiumchloride (mgcl2): Dit is een oplosbaar zout.
* koolstofdioxide (CO2): Dit is een gas dat uit de oplossing bubbelt.
* Water (H2O): Dit wordt gevormd door de reactie van de waterstofionen (H+) van het zuur en de hydroxide-ionen (OH-) uit het carbonaat.
De pH -verandering
* initiële pH: HCL is een sterk zuur, dus de initiële pH zal erg laag zijn (zuur).
* Final Ph: Naarmate de reactie vordert, reageren de waterstofionen (H+) van de HCl met de carbonaationen (CO3^2-) van het magnesiumcarbonaat. Dit vermindert de concentratie van H+ -ionen in de oplossing. De uiteindelijke pH is afhankelijk van de relatieve hoeveelheden zuur en gebruikte basis.
belangrijke overwegingen
* stoichiometrie: De exacte pH aan het einde is afhankelijk van de specifieke hoeveelheden HCl en MGCO3 die worden gebruikt. Als u gelijke mol van het zuur en de basis hebt, wordt de oplossing waarschijnlijk neutraal (pH 7) naarmate de reactie tot voltooiing gaat.
* Overtollige reactant: Als een reactant overtollig is, wordt de uiteindelijke pH bepaald door de overtollige reactant. Als er bijvoorbeeld overtollige HCL is, blijft de oplossing zuur.
Samenvattend:
De reactie van zoutzuur en magnesiumcarbonaat is een neutralisatiereactie. De pH van de oplossing zal veranderen van aanvankelijk zuur naar mogelijk neutraal of enigszins zuur, afhankelijk van de hoeveelheden van elke reactant.
 Wat gebeurt er bij een zuurgebaseerde reactie volgens de Arrhenius-definitie?
Wat gebeurt er bij een zuurgebaseerde reactie volgens de Arrhenius-definitie?  Hoogwaardige metaalgedoteerde amorfe IrOx als stabiele elektrokatalysator voor zure zuurstofontwikkelingsreactie
Hoogwaardige metaalgedoteerde amorfe IrOx als stabiele elektrokatalysator voor zure zuurstofontwikkelingsreactie  Hoe balanceer je al plus cl cu?
Hoe balanceer je al plus cl cu?  Is NAC2H3O2 en HCH3O2 een buffer in water?
Is NAC2H3O2 en HCH3O2 een buffer in water?  Alternatieve cementrecepten - Een recept voor eco-beton
Alternatieve cementrecepten - Een recept voor eco-beton
 Hoe wordt het proces genaamd waar een onderzoeksonderzoek wordt geaccepteerd als waar en wetenschappelijk?
Hoe wordt het proces genaamd waar een onderzoeksonderzoek wordt geaccepteerd als waar en wetenschappelijk?  Hoe de biodiversiteit verandert in een van 's werelds meest productieve oceaanecosystemen
Hoe de biodiversiteit verandert in een van 's werelds meest productieve oceaanecosystemen  Oceaanplastic dat de kusten van Chili ooit verstikte, nu in hoeden van Patagonië
Oceaanplastic dat de kusten van Chili ooit verstikte, nu in hoeden van Patagonië  Hoe burgerwetenschap onze zeeën redt
Hoe burgerwetenschap onze zeeën redt  NASA vindt zware waterdampconcentratie ringen oog van cycloon Amphan
NASA vindt zware waterdampconcentratie ringen oog van cycloon Amphan
Hoofdlijnen
- Wat gebeurt er in een halve cel?
- Wat doen wetenschappers die puur onderzoek doen?
- Welke producten ATP?
- Welk proces gebruiken heterozygote organismen om energie vrij te geven?
- Natuurlijke enzymen filteren hormoonverstorende chemicaliën uit rioolwater
- Mannelijke mammoeten vielen vaker in natuurlijke vallen en stierven, DNA-bewijs suggereert:
- De krachtpatser van cel genoemd. Waar cel al zijn energie vandaan haalt?
- Hoe beïnvloedt de structuur van DNA zijn functie?
- Wasberen lossen een eeuwenoude puzzel op, maar begrijpen ze die echt?
- Chemicaliën in het milieu:aandacht voor mengsels

- Engineered C. glutamicum-stam die in staat is glutaarzuur op hoog niveau te produceren uit glucose
- Chemici ontwikkelen een methode om verbindingen voor geneesmiddelen te synthetiseren
- Leven bevroren in de tijd onder een elektronenmicroscoop krijgt Nobelprijs
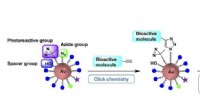
- Eenvoudig te monteren steigers van gouden nanodeeltjes dienen als moleculaire sonde
 Topologisch gecontroleerde multiskyrmions:onderzoekers stellen een nieuwe familie van quasideeltjes voor
Topologisch gecontroleerde multiskyrmions:onderzoekers stellen een nieuwe familie van quasideeltjes voor  Meervoudige aanval van virussen op bacteriën wijst op nieuwe manieren om infecties te bestrijden
Meervoudige aanval van virussen op bacteriën wijst op nieuwe manieren om infecties te bestrijden Spaanse steden beu barsten Airbnb-zeepbel
Spaanse steden beu barsten Airbnb-zeepbel Wat is het aantal vervangbare waterstofionen in H3PO4?
Wat is het aantal vervangbare waterstofionen in H3PO4?  Wat is de helderheid voor ster Sheraton?
Wat is de helderheid voor ster Sheraton?  Welke ecosysteemveranderingen kunnen worden teruggedraaid?
Welke ecosysteemveranderingen kunnen worden teruggedraaid?  Wat bestaat verder dan het zonnestelsel?
Wat bestaat verder dan het zonnestelsel?  Zijn door het Pentagon bevestigde UFO’s een bedreiging voor de nationale veiligheid?
Zijn door het Pentagon bevestigde UFO’s een bedreiging voor de nationale veiligheid?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

