
Wetenschap
Wat is het effect van een stoffendichtheid op zijn specifieke warmtecapaciteit?
Dit is waarom:
* Dichtheid is een maat voor hoeveel massa in een bepaald volume wordt verpakt. Het is in wezen hoe "dicht" een stof is.
* Specifieke warmtecapaciteit is een maat voor hoeveel energie nodig is om de temperatuur van een eenheidsmassa van een stof met één graad te verhogen. Het gaat erom hoeveel warmte een stof kan "vasthouden" voordat de temperatuur verandert.
Deze twee eigenschappen meten verschillende aspecten van een stof:
* Dichtheid: Richt zich op de * hoeveelheid materie * in een bepaalde ruimte.
* Specifieke warmtecapaciteit: Richt zich op de * energie die nodig is om de temperatuur * van een bepaalde hoeveelheid materie te veranderen.
Voorbeeld:
* lead heeft een hoge dichtheid (11,34 g/cm³) en een relatief lage specifieke warmtecapaciteit (0,128 J/g ° C).
* Water heeft een lagere dichtheid (1 g/cm³) maar een veel hogere specifieke warmtecapaciteit (4.184 J/g ° C).
Dit laat zien dat een dichte stof niet noodzakelijkerwijs een lage specifieke warmtecapaciteit heeft en vice versa.
factoren die specifieke warmtecapaciteit beïnvloeden:
* Moleculaire structuur: Complexe moleculen met meer trillingsmodi hebben hogere specifieke warmtecapaciteiten.
* intermoleculaire krachten: Sterkere intermoleculaire krachten (zoals waterstofbinding) vereisen meer energie om te breken en leiden dus tot hogere specifieke warmtecapaciteiten.
* Fase van materie: Vaste stoffen hebben over het algemeen lagere specifieke warmtecapaciteiten dan vloeistoffen, die op hun beurt lagere specifieke warmtecapaciteiten hebben dan gassen.
Concluderend, hoewel dichtheid en specifieke warmtecapaciteit beide fysische eigenschappen van stoffen zijn, zijn ze onafhankelijk van elkaar.
 IJswedging is een vorm van chemische verwering.
IJswedging is een vorm van chemische verwering.  Wat is een sterk zuur citroenzuur, salpeterzuur of fosforzuur?
Wat is een sterk zuur citroenzuur, salpeterzuur of fosforzuur?  Precisie-experimenten onthullen hiaten in de theorie van Van der Waals
Precisie-experimenten onthullen hiaten in de theorie van Van der Waals Wat is de molariteit van een oplossing die 125 g NaCl opgelost in 4,00 L -oplossing bevat?
Wat is de molariteit van een oplossing die 125 g NaCl opgelost in 4,00 L -oplossing bevat?  Een kaart van reacties helpt bij het controleren van moleculaire eigenschappen
Een kaart van reacties helpt bij het controleren van moleculaire eigenschappen
 Wat zijn twee ideeën over evolutie die door wetenschappers in de 18e eeuw werden voorgesteld?
Wat zijn twee ideeën over evolutie die door wetenschappers in de 18e eeuw werden voorgesteld?  Superhittegolven van 55 C komen op als de opwarming van de aarde doorzet
Superhittegolven van 55 C komen op als de opwarming van de aarde doorzet Herziene temperatuurrecord uit het Holoceen bevestigt de rol van broeikasgassen in de afgelopen millennia
Herziene temperatuurrecord uit het Holoceen bevestigt de rol van broeikasgassen in de afgelopen millennia Oase-effect in stadsparken kan bijdragen aan de uitstoot van broeikasgassen, studie vondsten
Oase-effect in stadsparken kan bijdragen aan de uitstoot van broeikasgassen, studie vondsten Hoe de VS hun belofte van Parijs zouden kunnen nakomen zonder het Witte Huis?
Hoe de VS hun belofte van Parijs zouden kunnen nakomen zonder het Witte Huis?
Hoofdlijnen
- Hoe verschillen Rickettsiae van Chlamydiae?
- Hoe cheeta's elkaar vinden na hun scheiding
- Science Fair Projectideeën voor tandheelkunde
- Zijn ziekteverwekkers bacteriën en schimmelsvirus?
- Hoe functioneert een sporangiofoor in de reproductie van schimmels?
- Welk bewijsmateriaal gebruiken wetenschappers om fylogenetische bomen te maken?
- Naarmate het klimaat warmer wordt, muizen morph
- Hoe worden de niet -functionele delen van het transcript genoemd?
- Een belangrijke reden waarom vrouwen stoppen met doctorale STEM-programma’s
- Een nieuw MXene-materiaal vertoont een buitengewoon afschermend vermogen tegen elektromagnetische interferentie

- Eenvoudige methode meet hoe lang bacteriën kunnen wachten op antibiotica
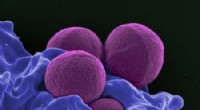
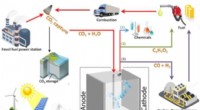
- Onderzoekers maken alcohol uit het niets
- De geheimen achter een griezelige fotografische techniek

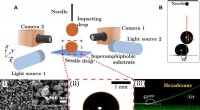
- Een sessiele druppel optillen van een superamfifoob oppervlak met behulp van een inslaande druppel
 Planten in de Noordpool
Planten in de Noordpool Wat is het gebruik van knopschilfers in houtachtige planten?
Wat is het gebruik van knopschilfers in houtachtige planten?  Natuurlijke of door de mens veroorzaakte aardbevingen? Nieuwe techniek kan het verschil maken
Natuurlijke of door de mens veroorzaakte aardbevingen? Nieuwe techniek kan het verschil maken  Noem en beschrijf de verschillende soorten bodems op verschillende plaatsen India?
Noem en beschrijf de verschillende soorten bodems op verschillende plaatsen India?  Snel een witte LED ontwerpen
Snel een witte LED ontwerpen Science Fair-experimenten met baking soda en water
Science Fair-experimenten met baking soda en water  Wat gebeurt er met de snelheid van fotosynthese als er geen regenval is?
Wat gebeurt er met de snelheid van fotosynthese als er geen regenval is?  Raad eens wat deze jonge dinosaurussen aten toen hun ouders niet keken
Raad eens wat deze jonge dinosaurussen aten toen hun ouders niet keken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

