
Wetenschap
Hoeveel covalente bindingen worden gevormd door silicium?
Silicium (SI) vormt vier Covalente bindingen.
Dit is waarom:
* Elektronenconfiguratie: Silicium heeft een elektronenconfiguratie van [NE] 3S² 3P². Het heeft vier elektronen in zijn buitenste schaal, wat de valentieschaal is.
* octetregel: Om een stabiele elektronenconfiguratie te bereiken (zoals de edelgassen), moet silicium nog vier elektronen krijgen. Het doet dit door zijn vier valentie -elektronen te delen met andere atomen en vier covalente bindingen te vormen.
* Voorbeeld: In siliciumdioxide (SIO₂) vormt elk siliciumatoom vier covalente bindingen met twee zuurstofatomen.
 Aanhoudende motregen bij temperaturen onder nul op Antarctica
Aanhoudende motregen bij temperaturen onder nul op Antarctica De uitstoot van lachgas kan erger worden naarmate het klimaat warmer wordt
De uitstoot van lachgas kan erger worden naarmate het klimaat warmer wordt Vrouwen lopen veertien keer zoveel kans om te sterven bij een klimaatramp dan mannen – dit is maar één manier waarop klimaatverandering gendergerelateerd is
Vrouwen lopen veertien keer zoveel kans om te sterven bij een klimaatramp dan mannen – dit is maar één manier waarop klimaatverandering gendergerelateerd is  Hugo, ik en iedereen:Doe mee aan de oorlog tegen plasticvervuiling
Hugo, ik en iedereen:Doe mee aan de oorlog tegen plasticvervuiling Schattingen van sneeuwmassa nu betrouwbaarder
Schattingen van sneeuwmassa nu betrouwbaarder
Hoofdlijnen
- Dode walvis verrast zwemmers op iconisch strand van Rio
- In een cel vormen de verwarde lange strengen DNA de?
- Papegaaien geven de voorkeur aan live videogesprekken boven het bekijken van vooraf opgenomen video's van andere vogels
- Wat is een andere naam voor een waarneembaar kenmerk of kenmerk van organisme?
- Wat zijn voordelen van eiwitten?
- Hoe evolueerden gewervelde dieren voor het eerst hun kaken?
- Nieuw inzicht in hoe de oorzakelijke genproducten van xeroderma pigmentosum de nauwkeurigheid van DNA-reparatie garanderen
- Waar denken sommige wetenschappers dat de eenvoudige bacteriën die ooit alleen de vorm van leven op aarde waren, ontstonden?
- Wanneer realiseerden wetenschappers zich dat archee verschilde van bacteriën?
- Nieuw proces voor het produceren van hoogspanningskathodes voor lithium-ionbatterijen

- Nieuwe gel beschermt eieren - en misschien ooit koppen - tegen schade

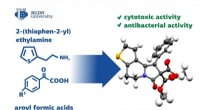
- Chemici ontwikkelen een methode om verbindingen voor geneesmiddelen te synthetiseren
- Een concrete stap in de richting van nul CO2-uitstoot bij de cementproductie

- Reactie-inzichten helpen bij het maken van duurzame vloeibare brandstoffen
 UA maakt deel uit van een groep die ontrafelt hoe de hersenen het geheugen beheren
UA maakt deel uit van een groep die ontrafelt hoe de hersenen het geheugen beheren  In welk gebied van het interieur neemt warmte toe om te wijzen dat rotsen kunnen beginnen smelten?
In welk gebied van het interieur neemt warmte toe om te wijzen dat rotsen kunnen beginnen smelten?  De voorgestelde richtlijnen voor seksuele voorlichting in Engeland druisen in tegen het bewijsmateriaal en kunnen heel goed tot schade leiden
De voorgestelde richtlijnen voor seksuele voorlichting in Engeland druisen in tegen het bewijsmateriaal en kunnen heel goed tot schade leiden  Uber draagt mogelijk meer transportvervuiling bij dan oplossing:studie
Uber draagt mogelijk meer transportvervuiling bij dan oplossing:studie Waarom verandert de vorm van een rode bloedcel in verschillende oplossingen?
Waarom verandert de vorm van een rode bloedcel in verschillende oplossingen?  Wat is de mogelijkheid om kracht uit te oefenen voor een korte tijd genoemd?
Wat is de mogelijkheid om kracht uit te oefenen voor een korte tijd genoemd?  Waarom is zonne -energie een overvloedige hernieuwbare bron?
Waarom is zonne -energie een overvloedige hernieuwbare bron?  Pre-blootstelling met helium remt de permeatie van waterstofisotopen in wandmaterialen
Pre-blootstelling met helium remt de permeatie van waterstofisotopen in wandmaterialen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

