
Wetenschap
Welke vorm verwacht je van NO2 - ion?
* Lewis -structuur: Het centrale stikstofatoom heeft drie elektronendomeinen:de ene dubbele binding aan een zuurstofatoom, de ene enkele binding aan een ander zuurstofatoom en het ene eenzaam paar.
* vSEPR -theorie: VSEPR (Valent Shell Electron Pair Repulsion) Theory voorspelt dat elektronendomeinen rond een centraal atoom zich zullen regelen om afstoting te minimaliseren. Drie elektronendomeinen resulteren in een trigonale vlakke elektronengeometrie.
* Moleculaire vorm: Het enige paar op stikstof oefent een sterkere afstoting uit dan de bindingsparen en duwt de twee zuurstofatomen dichter bij elkaar. Dit resulteert in een gebogen of hoekige moleculaire vorm.
Samenvattend: Het No₂⁻ -ion heeft een gebogen moleculaire vorm vanwege de aanwezigheid van een eenzaam paar op het centrale stikstofatoom.
 Hoe ID Mountain Lion Poop
Hoe ID Mountain Lion Poop  Hoe is het leven op aarde ontstaan?
Hoe is het leven op aarde ontstaan?  Groene straten:waarom het beschermen van stadsparken en struiken van cruciaal belang is naarmate onze steden dichter worden
Groene straten:waarom het beschermen van stadsparken en struiken van cruciaal belang is naarmate onze steden dichter worden  Versneld drogen verhoogt de kans op bosbranden in de hele staat in Texas
Versneld drogen verhoogt de kans op bosbranden in de hele staat in Texas Baby's in kinderwagens kunnen worden blootgesteld aan meer dan twee keer zoveel vervuiling dan volwassenen
Baby's in kinderwagens kunnen worden blootgesteld aan meer dan twee keer zoveel vervuiling dan volwassenen
Hoofdlijnen
- Hoe verschilt een orgel van het systeem?
- De erfelijkheidsinformatie voor een bepaalde eigenschap is over het algemeen wat?
- Wat zit er in een naam? Big Data onthult onderscheidende patronen in hogeronderwijssystemen
- Wat is er anders tussen de twee soorten gisting?
- Wie stelde het idee van overleven die fittest is een theorie -evolutie voor?
- Wie was de wetenschapper die het bestaan van kern toonde?
- 5 stadia van mitose
- Waar komt biogene vandaan?
- Welke stoffen hebben een netto beweging in de mitochondria?
- Natuurkundig team onderzoekt invloed van ionen op atomaire bewegingen

- Verdunning detecteren:nieuwe experimentele en theoretische benaderingen duiken in de pool van organellen van membranen

- Zeldzame aarde-orthoferriet LnFeO3-nanodeeltjes voor bio-imaging
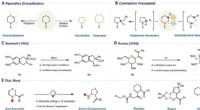
- Een reactie die zwavel verwijdert, stikstof- of zuurstofatomen uit zesledige ringen die alleen blauw licht gebruiken
- Zuurstof geven aan de kwestie van luchtkwaliteit

 Bioprospectie van het onbekende:hoe bacteriële enzymen gecodeerd door onbekende genen kunnen helpen bij het opruimen van vervuiling
Bioprospectie van het onbekende:hoe bacteriële enzymen gecodeerd door onbekende genen kunnen helpen bij het opruimen van vervuiling  Wat is materiaaloverdrachtsenergie gemakkelijk?
Wat is materiaaloverdrachtsenergie gemakkelijk?  Aceton en piepschuim Experiment
Aceton en piepschuim Experiment  Onderzoeksteam bestudeert geologie van bosbranden
Onderzoeksteam bestudeert geologie van bosbranden Wat zijn de kleinste sterren die in het zonnestelsel worden genoemd?
Wat zijn de kleinste sterren die in het zonnestelsel worden genoemd?  Hoe roofzuchtig plankton moderne ecosystemen creëerde na Snowball Earth
Hoe roofzuchtig plankton moderne ecosystemen creëerde na Snowball Earth Sneller dan de snelheid van het geluid:nieuw besturingssysteem heeft alles wat nodig is om experimentele vliegtuigen te besturen
Sneller dan de snelheid van het geluid:nieuw besturingssysteem heeft alles wat nodig is om experimentele vliegtuigen te besturen  Hoe wordt gas gewonnen uit schalie?
Hoe wordt gas gewonnen uit schalie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

