
Wetenschap
Wat is de vergelijking voor wanneer ammoniak geïoniseerd oplost in water?
nH₃ (aq) + h₂o (l) ⇌ nH₄⁺ (aq) + oh⁻ (aq)
Hier is een uitsplitsing:
* NH₃ (aq): Ammoniak opgelost in water (waterige oplossing).
* h₂o (l): Water in zijn vloeibare toestand.
* NH₄⁺ (aq): Ammoniumion, gevormd wanneer ammoniak een proton (H⁺) van water krijgt.
* oh⁻ (aq): Hydroxide -ion, gevormd wanneer water een proton (H⁺) verliest aan ammoniak.
Verklaring:
Ammoniak fungeert als een zwakke basis in water. Het accepteert een proton uit water, vormt het ammoniumion (NH₄⁺) en laat een hydroxide -ion achter (OH⁻). De reactie is omkeerbaar, wat betekent dat sommige ammoniumionen hun proton terug kunnen schenken aan hydroxide -ionen, het hervormen van ammoniak en water.
Opmerking: De dubbele pijl (⇌) geeft aan dat de reactie in evenwicht is, wat betekent dat deze tegelijkertijd in beide richtingen verloopt. De positie van het evenwicht ligt links, wat betekent dat ammoniak een zwakke basis is en slechts een kleine hoeveelheid ervan in water ioniseert.
 Wat zijn 5 hoofdstappen van de wetenschappelijke methode?
Wat zijn 5 hoofdstappen van de wetenschappelijke methode?  Welk materiaal is tegelijkertijd een vaste stof en vloeistof?
Welk materiaal is tegelijkertijd een vaste stof en vloeistof?  Hoeveel covalente bindingen worden gevormd door silicium?
Hoeveel covalente bindingen worden gevormd door silicium?  Wat zijn tactische kernwapens? Veiligheidsexpert legt uit en beoordeelt wat ze betekenen voor de oorlog in Oekraïne
Wat zijn tactische kernwapens? Veiligheidsexpert legt uit en beoordeelt wat ze betekenen voor de oorlog in Oekraïne  Hoeveel is 5 milliliter vloeistoffen?
Hoeveel is 5 milliliter vloeistoffen?
 Welk deel van de aarde vallen objecten op?
Welk deel van de aarde vallen objecten op?  Microplastics:geen klein probleem voor filtervoedende oceaanreuzen
Microplastics:geen klein probleem voor filtervoedende oceaanreuzen Een duurzaam noordpoolgebied moet inheemse groepen omvatten
Een duurzaam noordpoolgebied moet inheemse groepen omvatten Onderzoekers tonen aan dat grotere plantengemeenschappen productiever zijn en gevoeliger voor klimaatopwarming
Onderzoekers tonen aan dat grotere plantengemeenschappen productiever zijn en gevoeliger voor klimaatopwarming  Wat een opwarmende wereld betekent voor dodelijke wervelstormen en het soort stormen dat ze voortbrengt
Wat een opwarmende wereld betekent voor dodelijke wervelstormen en het soort stormen dat ze voortbrengt
Hoofdlijnen
- Hoe bestrijden witte bloedcellen bacteriën?
- Wat is het nuttige micro -organisme dat aanwezig is in wrongel?
- Een driedimensionaal model van een plantencel maken met labels
- Onderzoek onthult de sleutelrol van de communicatie tussen planten en bacteriën bij de assemblage van een gezond plantenmicrobioom
- Welke informatie wordt overgedragen van de kern naar ribosoom geroepen?
- Wat gebeurt er als we zin orgel hebben?
- Waarom is het Golgi-apparaat belangrijk en welke taak heeft het apparaat ons in ons lichaam geholpen?
- Gestandaardiseerde metadata voor biologische monsters zouden het potentieel van collecties kunnen ontsluiten
- Wat doet de biosfeer met mensen?
- Ionengeleidend polymeer cruciaal voor het verbeteren van neuromorfe apparaten

- Onderzoekers remmen de groei van kankercellen met verbindingen die planten beschermen tegen roofdieren
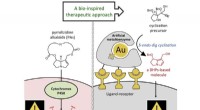
- Fluorescerende sondes bewijzen het bestaan van celmembraanstructuren van lipidenvlotten
- Team krijgt inzicht in de oxidelaag van roestvrij staal

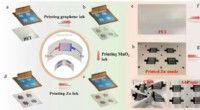
- Hoge veiligheid, flexibele en schaalbare oplaadbare planaire microbatterijen
 Waarom wordt het kwikelement kwik genoemd?
Waarom wordt het kwikelement kwik genoemd?  Welke uitspraken over activeringsenergie zijn correct?
Welke uitspraken over activeringsenergie zijn correct?  Zwitserland in epicentrum van cryptocurrency-revolutie
Zwitserland in epicentrum van cryptocurrency-revolutie Verwijderen van Mucus
Verwijderen van Mucus Ultrasnelle mode charmeert jong ondanks schadelijke omgeving
Ultrasnelle mode charmeert jong ondanks schadelijke omgeving Wat is de rol van experiment bij het vaststellen van principiële conserveringsenergie?
Wat is de rol van experiment bij het vaststellen van principiële conserveringsenergie?  Superzware zwarte gaten in stervende sterrenstelsels gedetecteerd in het vroege heelal
Superzware zwarte gaten in stervende sterrenstelsels gedetecteerd in het vroege heelal Welk type informatie wordt gepresenteerd door een wetenschapper die reden heeft die een bepaalde manier presenteert?
Welk type informatie wordt gepresenteerd door een wetenschapper die reden heeft die een bepaalde manier presenteert?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

