
Wetenschap
Onderzoekers remmen de groei van kankercellen met verbindingen die planten beschermen tegen roofdieren
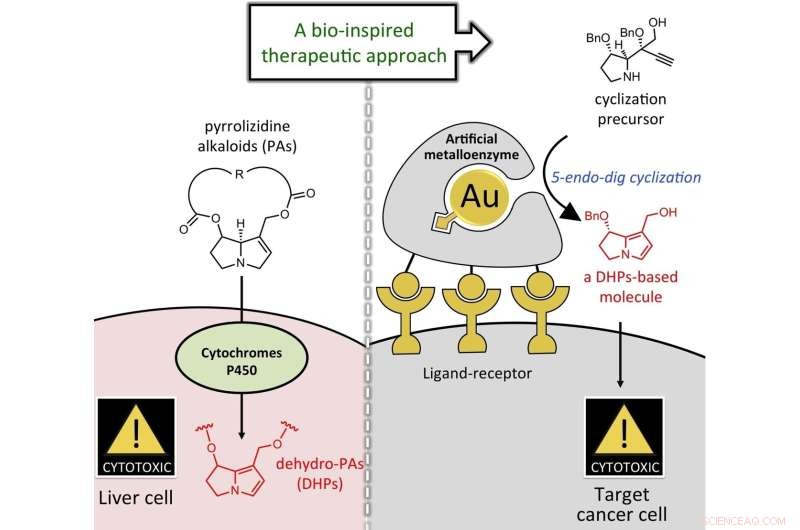
Grafisch abstract. Krediet:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202205541
Onderzoekers in Japan zijn erin geslaagd de groei van kankercellen te remmen met behulp van pyrrolizidine-alkaloïde, een bestanddeel van plantaardige oorsprong waarvan eerder werd gedacht dat het te giftig was om toe te dienen.
Pyrrolizidine-alkaloïden worden aangetroffen in ongeveer 6000 plantensoorten, waaronder de madeliefjes- en bonenfamilies. In planten beschermen ze planten tegen roofdieren; bij mensen hebben ze echter antibacteriële en antitumor eigenschappen, waardoor ze bruikbaar zijn voor kruidengeneeskunde. Vroege studies meldden dat pyrrolizidine-alkaloïden kankercellen konden doden, maar het onderzoek werd stopgezet omdat ze ook leverschade veroorzaakten.
"Het probleem van giftig zijn voor de lever is onlosmakelijk verbonden met het werkingsmechanisme van pyrrolizidine-alkaloïden", legt hoofdauteur professor Satoshi Yokoshima uit. "Pyrrolizidine-alkaloïden vertonen alleen toxiciteit wanneer ze in het lichaam worden gemetaboliseerd en worden omgezet in hun 'actieve vorm' die de pyrroolstructuur bevat. De actieve vorm beschadigt het DNA van de kankercel, waardoor het niet kan worden gereproduceerd, maar het maakt ze ook schadelijk voor nucleïnezuren en eiwitten in de lever."
Professor Yokoshima van de Graduate School of Pharmaceutical Science, Nagoya University, onderzocht samen met professor Katsunori Tanaka van het Tokyo Institute of Technology en RIKEN de mogelijkheid om de proliferatie van kankercellen te remmen zonder toxiciteit. De onderzoekers dienden een moleculaire voorloper van pyrrolizidine-alkaloïde toe met een andere structuur. Vervolgens hebben ze het omgezet in het actieve lichaam dat de pyrroolstructuur bevat in de buurt van kankercellen om schade te minimaliseren. Hun bevindingen zijn gepubliceerd in Angewandte Chemie International Edition .
"Ik ben geïnteresseerd in de structuur van natuurlijke producten", legt professor Yokoshima uit. "Het is leuk om ze te synthetiseren. Misschien zien we iets nieuws in de organische chemie of ontwikkelen we een nieuwe methode. In dit experiment hebben we een nieuwe verbinding ontworpen met een andere structuur als voorloper van de actieve vorm. Omdat het het lichaam niet schaadde , hebben we het geïntroduceerd en vervolgens omgezet in de actieve vorm met behulp van een goudkatalysator in de aanwezigheid van kanker."
Om goudkatalysatoren in het lichaam te introduceren, wendde het team zich tot professor Tanaka van RIKEN die een goudkatalysator had ondersteund op albumine, een eiwit dat in bloed wordt aangetroffen. Ze introduceerden ook meerdere suikerketens op het oppervlak van albumine, gebruikmakend van het feit dat suikerketens het oppervlak van kankercellen herkennen. Het albumine bond aan de kankercellen en de reactie vond plaats in de buurt van kankercellen, waardoor de schade aan andere cellen werd beperkt.
Het team bevestigde de conversie naar de actieve vorm die de pyrroolstructuur bevat. Dit was het bewijs van 'synthese ter plaatse', wat betekent dat de actieve vorm in de buurt van kankercellen is gemaakt om schade aan het lichaam te beperken. Ze bevestigden ook een opmerkelijke groeiremming van de beoogde kankercellen.
"Pyrrolizidine-alkaloïden zijn giftig voor de lever, maar deze methode kan toxiciteit voorkomen", zegt professor Yokoshima. "Als we dit in vivo kunnen toepassen, zou het een nieuwe methode voor kankerbehandeling kunnen zijn. We hopen dat andere potentiële behandelingen tegen kanker die werden stopgezet vanwege toxiciteitsproblemen, opnieuw kunnen worden getest als mogelijke behandelingen met behulp van de on-site synthesemethode. Ik hoop dat deze methode biedt inzichten die anderen kunnen gebruiken om hun eigen medicijnen te maken." + Verder verkennen
Activering van prodrug met behulp van in eiwit omhulde goudkatalysator
 Chemisch jongleren met drie deeltjes
Chemisch jongleren met drie deeltjes Chlorofyl verwijderen van bladeren
Chlorofyl verwijderen van bladeren Gesprek tussen een bioloog en een filosoof:is de mens een halfgod geworden?
Gesprek tussen een bioloog en een filosoof:is de mens een halfgod geworden? Onderzoekers ontdekken dat gel littekenweefsel vermindert na operatie bij dieren
Onderzoekers ontdekken dat gel littekenweefsel vermindert na operatie bij dieren Wetenschappers ontwikkelen strategie om afzonderlijke atomen te stabiliseren met ionische vloeistof als elektronische stabilisator
Wetenschappers ontwikkelen strategie om afzonderlijke atomen te stabiliseren met ionische vloeistof als elektronische stabilisator
 Sneeuwonderzoek vult hiaat in inzicht in Arctisch klimaat
Sneeuwonderzoek vult hiaat in inzicht in Arctisch klimaat Duiker filmt afvalland in de wateren van Bali
Duiker filmt afvalland in de wateren van Bali Zelfs zonder het schone energieplan, VS kunnen emissiereducties in de Overeenkomst van Parijs bereiken
Zelfs zonder het schone energieplan, VS kunnen emissiereducties in de Overeenkomst van Parijs bereiken Kleiner dan verwacht fytoplankton kan betekenen dat er minder koolstof wordt vastgelegd op de zeebodem
Kleiner dan verwacht fytoplankton kan betekenen dat er minder koolstof wordt vastgelegd op de zeebodem Wat is een anaerobe omgeving?
Wat is een anaerobe omgeving?
Hoofdlijnen
- Waarom kunnen we ons niet herinneren dat we baby's waren?
- Hoe zijn cellen, weefsels en organen aan elkaar gerelateerd?
- Infectieziekten:CTRL + ALT + Delete
- Karkas van Noord-Atlantische rechtse walvis gespot in Massachusetts
- Waar bevinden zich lipiden in het lichaam?
- Your Body On: A Horror Movie
- Pareidolie:waarom we in bijna alles gezichten zien
- De geboorte van een jongere broer of zus activeert langdurige stressreacties bij jonge bonobo's
- Maakt Koud U Slaperig?
- Optisch pincet met aerosol verbetert het begrip van deeltjes in de lucht

- Onderzoekers optimaliseren materiaalontwerp met behulp van computationele technologieën

- Infectie voorkomen met een verbeterde zilvercoating voor medische hulpmiddelen

- Metabolisch gemanipuleerde bacterie produceert luteïne
- Zelfreinigend beton kan gebouwen er als nieuw uit laten zien

 De rol van enzymen in chemische reacties
De rol van enzymen in chemische reacties Zuurstof-vacature-gemedieerde katalyse stimuleert directe methanisering van biomassa
Zuurstof-vacature-gemedieerde katalyse stimuleert directe methanisering van biomassa Niet-levende dingen in een bosecosysteem
Niet-levende dingen in een bosecosysteem Speeksel kan smaakvoorkeuren beïnvloeden
Speeksel kan smaakvoorkeuren beïnvloeden Vijftig jaar geleden, Jocelyn Bell ontdekte pulsars en veranderde onze kijk op het universum
Vijftig jaar geleden, Jocelyn Bell ontdekte pulsars en veranderde onze kijk op het universum Pentagon:$ 10 miljard cloudcontract dat Amazon afsnauwde was legaal
Pentagon:$ 10 miljard cloudcontract dat Amazon afsnauwde was legaal Voors en tegens van Algae Biodiesel
Voors en tegens van Algae Biodiesel  E. coli gebruiken om bioproducten te maken, zoals biodiesel, op een kosteneffectieve manier
E. coli gebruiken om bioproducten te maken, zoals biodiesel, op een kosteneffectieve manier
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

