
Wetenschap
Wat is de evenwichtige vergelijking voor de reactie van magnesiummetaal en zoutzuur?
mg (s) + 2HCl (aq) → mgcl₂ (aq) + h₂ (g)
Dit is wat er gebeurt:
* mg (s) :Magnesiummetaal is de vaste reactant.
* HCl (aq) :Zoutzuur is de waterige reactant.
* mgcl₂ (aq) :Magnesiumchloride is het waterige product.
* h₂ (g) :Waterstofgas is het gasvormige product.
Verklaring:
* Magnesium (mg) is reactiever dan waterstof (H) en verplaatst het van zoutzuur (HCL).
* De magnesiumatomen reageren met de waterstofionen (H+) van het zuur, waardoor magnesiumionen (mg²+) en waterstofgas (H₂) worden gevormd.
* De chloride-ionen (Cl-) blijven in oplossing, combineren met de magnesiumionen om magnesiumchloride te vormen (mgcl₂).
Belangrijke opmerking: Deze reactie is exotherme, wat betekent dat het warmte vrijgeeft en ervoor zorgt dat de oplossing warm wordt.
 Wanneer wordt gezegd dat een samengestelde formule -formule molecuul is?
Wanneer wordt gezegd dat een samengestelde formule -formule molecuul is?  Zal specifieke warmte van 50 g een stof hetzelfde zijn als of groter dan 10 stof?
Zal specifieke warmte van 50 g een stof hetzelfde zijn als of groter dan 10 stof?  Nieuwe methode ontdekt om eiwitten in menselijke cellen te bekijken
Nieuwe methode ontdekt om eiwitten in menselijke cellen te bekijken Wat wordt een binding gevormd door de aantrekkingskracht tussen positief geladen metaalionen en elektronen eromheen?
Wat wordt een binding gevormd door de aantrekkingskracht tussen positief geladen metaalionen en elektronen eromheen?  Hoeveel covalente bindingen verbinden de atomen in een ammoniakmolecuul (NH3)?
Hoeveel covalente bindingen verbinden de atomen in een ammoniakmolecuul (NH3)?
 Kustaanpassing tegen zeespiegelstijging is economisch zinvol
Kustaanpassing tegen zeespiegelstijging is economisch zinvol Drawins theorie van natuurlijke selectie en zijn onderdelen?
Drawins theorie van natuurlijke selectie en zijn onderdelen?  Waarom hebben niet meer steden groene daken nodig?
Waarom hebben niet meer steden groene daken nodig?  Zorgen toeristenboten voor stress bij walvissen? Onderzoekers vinden
Zorgen toeristenboten voor stress bij walvissen? Onderzoekers vinden  Bronnen van dodelijke luchtvervuiling in de Verenigde Staten identificeren
Bronnen van dodelijke luchtvervuiling in de Verenigde Staten identificeren
Hoofdlijnen
- De afnemende populaties van koninginnenschelpen zijn gefragmenteerd en dat verandert het natuurbeschermingsspel
- Welk type RNA draagt aminozuren naar de vertaalsite?
- Onderzoekers tonen aan dat de natuur haar meest vitale DNA behoudt door te multitasken
- Manitobas goudvleugelzangers:'s werelds laatste pure populatie die wordt geraakt door lokale en verre instandhoudingsproblemen
- Wat heeft Virchow bijgedragen aan de celtheorie?
- Wat is een gen en wat doet het?
- Wat zegt een hoofdletter over genen?
- Is er een psychologische reden waarom mensen gemeen zijn op internet?
- Noem de 2 dingen die meedoen om een zaadje te maken?
- Maggot-analyse wordt moleculair voor forensische zaken

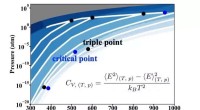
- Onder verschillende omstandigheden onderzoeken hoe oppervlakken veranderen in contact met reactieve gasfasen
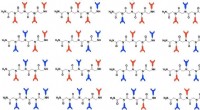
- Deze kunstmatige eiwitten hebben een stevige greep op metaal
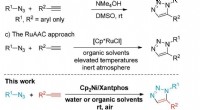
- Team presenteert nieuwe synthesemethode voor klikchemie
- Biologisch afbreekbare glitter en vervuilende microalgen:de nieuwe materialen geïnspireerd door de natuur

 Hoe kwamen mensen te weten over elektriciteit?
Hoe kwamen mensen te weten over elektriciteit?  Regering stelt voor om Fukushima-water vrij te laten in zee of in de lucht
Regering stelt voor om Fukushima-water vrij te laten in zee of in de lucht Vijftig simulaties van de 'Really Big One' laten zien hoe een aardbeving met een kracht van 9,0 Cascadia zou kunnen verlopen
Vijftig simulaties van de 'Really Big One' laten zien hoe een aardbeving met een kracht van 9,0 Cascadia zou kunnen verlopen  Waarom zijn luchtgedroogde handdoeken zo stijf?
Waarom zijn luchtgedroogde handdoeken zo stijf? Gameten zijn haploïd terwijl somatische cellen diploïd Wat is het verschil tussen een cel en cel?
Gameten zijn haploïd terwijl somatische cellen diploïd Wat is het verschil tussen een cel en cel?  Politieke opvattingen hebben een beperkte invloed op hoe we klimaatafwijkingen waarnemen, zo blijkt uit onderzoek
Politieke opvattingen hebben een beperkte invloed op hoe we klimaatafwijkingen waarnemen, zo blijkt uit onderzoek  Wil je daar groen bij?
Wil je daar groen bij?  Wat is de som van alle chemische processen die plaatsvinden in een organisme?
Wat is de som van alle chemische processen die plaatsvinden in een organisme?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

