
Wetenschap
Als een koperen spiraal wordt geplaatst in de oplossing van zilvernitraatkristallen op het oppervlak sterk oplosbaar gegenereerd?
Dit is wat er gebeurt:
* koper (Cu) is meer reactief dan zilver (Ag). Dit betekent dat koper gemakkelijk zijn elektronen zal opgeven om ionen te vormen.
* zilvernitraat (Agno3) is een oplosbaar zout. Wanneer opgelost in water, vormt het zilverionen (Ag+) en nitraationen (NO3-).
* Wanneer een koperen spoel in de zilvernitraatoplossing wordt geplaatst, verliezen de koperatomen elektronen en worden koperionen (Cu2+). Deze koperionen gaan dan in de oplossing.
* tegelijkertijd, zilverionen (Ag+) van de oplossingsversterking worden elektronen en worden zilveren atomen (Ag). Deze zilveren atomen deponeren op het oppervlak van de koperen spoel en vormen de zilveren kristallen die je ziet.
De chemische vergelijking voor deze reactie is:
Cu (s) + 2Agno3 (aq) → Cu (No3) 2 (aq) + 2ag (s)
Sleutelpunten:
* De reactie is spontaan Omdat koper reactiever is dan zilver.
* De oplossing wordt blauw Vanwege de aanwezigheid van koper (II) nitraat (Cu (NO3) 2), wat een oplosbaar zout is.
* De zilveren kristallen die vormen zijn onoplosbaar in water.
Laat het me weten als je nog meer vragen hebt!
 Wat is een kenmerk van sterk zuur?
Wat is een kenmerk van sterk zuur?  In kokende watermoleculen beweegt uit elkaar en ontsnappen in de vorm van damp die het proces wordt genoemd?
In kokende watermoleculen beweegt uit elkaar en ontsnappen in de vorm van damp die het proces wordt genoemd?  Lost suiker sneller op in koud of heet water?
Lost suiker sneller op in koud of heet water?  Waarom smeltpunt van NaCl is veel hoger dan CH4?
Waarom smeltpunt van NaCl is veel hoger dan CH4?  De eerste chemicus die de wet van constante samenstelling formeel vermeldde, was?
De eerste chemicus die de wet van constante samenstelling formeel vermeldde, was?
 Hoe insecten hun vleugels beheersen:de mysterieuze mechanica van insectenvluchten
Hoe insecten hun vleugels beheersen:de mysterieuze mechanica van insectenvluchten  Stijgende zeeën zullen miljoenen mensen verdrijven - en Australië moet er klaar voor zijn
Stijgende zeeën zullen miljoenen mensen verdrijven - en Australië moet er klaar voor zijn Het leven in het water:waarom kikkersoorten overdag genen hielden die aangepast waren aan nachtzicht
Het leven in het water:waarom kikkersoorten overdag genen hielden die aangepast waren aan nachtzicht  Risico's voor tsunami's herkennen
Risico's voor tsunami's herkennen Waarom is biodiversiteit belangrijk?
Waarom is biodiversiteit belangrijk?
Hoofdlijnen
- Het publiek is minder bang voor haaien als ze hun gedrag begrijpen
- Als een soort niet over voldoende genenpool beschikt,
- Welk lichaamssysteem reguleert activiteiten door zenuwimpulsen?
- Onderzoekers concentreren zich op de manier waarop bacteriën voedselvergiftiging veroorzaken
- Kan pizzakruid winterbraakziekte voorkomen?
- Hoe kleine watermonsters echt grote dieren kunnen vinden
- Wat is de wetenschappelijke term van LPG?
- Hoe zijn de reproductieve organen of een mannelijk en vrouwelijk hetzelfde hoe ze verschillen?
- Zeevruchten met een ecolabel zijn niet altijd wat het lijkt
- Nieuw composietmateriaal heeft potentieel voor medisch gebruik

- Onderzoeksteam ontgrendelt nieuwe methode voor het 3D-printen van complexe, functionele componenten voor zachte robotica

- Sporen van opiaten gevonden in oud Cypriotisch schip

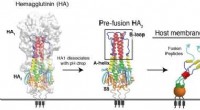
- Onderzoekers vinden nieuwe manier om griepvirus aan te pakken
- Onderzoekers ontwikkelen extreem gevoelige waterstofsensor

 Hoe wordt water uit de natuur gehaald?
Hoe wordt water uit de natuur gehaald?  Lopen mensen op de korst van de aarde?
Lopen mensen op de korst van de aarde?  Waarom laten mensen twee sets tanden groeien? Deze buideldieren herschrijven het verhaal van de tandevolutie
Waarom laten mensen twee sets tanden groeien? Deze buideldieren herschrijven het verhaal van de tandevolutie  Wat is een type turbine dat wordt gebruikt om de energie bewegende lucht vast te leggen?
Wat is een type turbine dat wordt gebruikt om de energie bewegende lucht vast te leggen?  Onderzoekers tonen aan dat neutrino's niet alleen volledige treffers kunnen veroorzaken, maar ook 'vluchtige slagen'
Onderzoekers tonen aan dat neutrino's niet alleen volledige treffers kunnen veroorzaken, maar ook 'vluchtige slagen'  Wetenschappelijke theorieën zijn niet louter gissingen - om te overleven moeten ze werken
Wetenschappelijke theorieën zijn niet louter gissingen - om te overleven moeten ze werken Hoe de functie te vinden in Math
Hoe de functie te vinden in Math Waarom is het kookpunt van H2O veel hoger dan dat van h2se?
Waarom is het kookpunt van H2O veel hoger dan dat van h2se?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

