
Wetenschap
Wat is de vergelijking voor zilvernitraat en koperchloride?
2AGNO₃ (aq) + cucl₂ (aq) → 2Agcl (s) + cu (no₃) ₂ (aq)
Dit is wat de vergelijking ons vertelt:
* (aq) geeft aan dat de stof is opgelost in water (waterige oplossing).
* (s) geeft aan dat de stof een vast neerslag is.
Verklaring:
* Zilvernitraat en koperchloride zijn beide oplosbare ionische verbindingen, wat betekent dat ze zich in hun ionen dissociëren wanneer ze in water worden opgelost.
* De zilverionen (Ag⁺) van zilvernitraat reageren met de chloride -ionen (CL⁻) van koperchloride om zilverchloride (AgCl) te vormen, die onoplosbaar is in water en neerslaat als een witte vaste stof.
* De resterende ionen, koper (II) ionen (Cu²⁺) en nitraationen (NO₃⁻), combineren om kopernitraat (Cu (No₃) ₂) te vormen, die in water opgelost blijft.
belangrijke opmerkingen:
* Deze reactie wordt vaak gebruikt om neerslagreacties en het concept van oplosbaarheidsregels aan te tonen.
* De reactie produceert een wit neerslag van zilverchloride, dat vaak wordt gebruikt in fotografie en andere toepassingen.
 Hoe de pH te meten met behulp van waterstofelektrode?
Hoe de pH te meten met behulp van waterstofelektrode?  Welke samengestelde ammoniak bevat drie waterstofatomen voor elke atoomnitrgen, dus de chemische formule is?
Welke samengestelde ammoniak bevat drie waterstofatomen voor elke atoomnitrgen, dus de chemische formule is?  Hoeveel mol in 2,12 g natriumcarbonaat?
Hoeveel mol in 2,12 g natriumcarbonaat?  Welk element wordt gevonden in alle organische verbindingen en levende orginismen?
Welk element wordt gevonden in alle organische verbindingen en levende orginismen?  Bevatten zure en basische oplossingen ionen?
Bevatten zure en basische oplossingen ionen?
Hoofdlijnen
- Hoe kan obesitas genetisch zijn?
- Gastheer-, management- of microbiële eigenschappen:welke is dominant in de assemblage van het plantenmicrobioom?
- Onder de motorkap:hoe omgeving en genomen op elkaar inwerken bij de ontwikkeling van planten
- Welke koolhydraten vormt de celwallof planten?
- Hoe celprocessen beschadigde eiwitten verzamelen en dumpen
- Wat is onderzoekswetenschap?
- Waarom zijn sommige slangen zo giftig?
- Welke monosacharide is een bouwsteen van de muur van de plantencel?
- Welke uitspraak beschrijft dit reproductiepatroon het beste?
- Nieuwe methode versnelt ontwikkeling medicatie

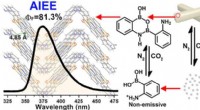
- Nieuw door aggregatie geïnduceerd aromatisch molecuul met verbeterde emissie ontdekt
- Fluorescerende sondes bewijzen het bestaan van celmembraanstructuren van lipidenvlotten
- Wetenschappers onthullen routekaart om de ontwikkeling van osteoporosebehandeling te ondersteunen

- Harde magnetische coatings voor zeer nauwkeurige microscopie

 Afbeelding:Cygnus-ruimtevaartuig nadert ISS bij zonsondergang
Afbeelding:Cygnus-ruimtevaartuig nadert ISS bij zonsondergang Hoe topografie beïnvloeden soortenverdeling?
Hoe topografie beïnvloeden soortenverdeling?  In welke chemische familie zit waterstof?
In welke chemische familie zit waterstof?  Nobelprijswinnaar wil wereldwijde milieurechtbank
Nobelprijswinnaar wil wereldwijde milieurechtbank Hoe diversifiëren en fylogenetisch correleren functionele eigenschappen voor co-voorkomende understory-soorten in boreale bossen?
Hoe diversifiëren en fylogenetisch correleren functionele eigenschappen voor co-voorkomende understory-soorten in boreale bossen? Hoe zou u het uiterlijk van het DNA -molecuul beschrijven?
Hoe zou u het uiterlijk van het DNA -molecuul beschrijven?  Nieuw onderzoek laat zien hoe planten ziekten bestrijden
Nieuw onderzoek laat zien hoe planten ziekten bestrijden  Ontdek hoe wapens werken
Ontdek hoe wapens werken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

