
Wetenschap
Waarom vormt chloorgas zich bij de positieve elektrode?
1. Oxidatie bij de anode: De anode is waar oxidatie optreedt. Dit betekent dat elektronen verloren gaan van de soort die aanwezig is in de elektrode.
2. De neiging van chloride -ionen om elektronen te verliezen: Chloride-ionen (Cl-) hebben een sterke neiging om elektronen te verliezen en chlooratomen te worden. Dit komt omdat chloor een zeer elektronegatief element is, wat betekent dat het een sterke aantrekkingskracht heeft op elektronen.
3. Vorming van chloorgas: Wanneer chloride -ionen elektronen verliezen bij de anode, worden ze chlooratomen. Deze chlooratomen combineren vervolgens met elkaar om chloorgas te vormen (CL2):
2CL- → CL2 + 2E-
Algemeen proces:
Tijdens de elektrolyse van een oplossing die chloride -ionen bevat, vindt het volgende proces plaats bij de anode:
* Chloride-ionen (Cl-) migreren naar de positieve anode.
* Chloride -ionen verliezen elektronen (oxidatie) en worden chlooratomen.
* Chlooratomen combineren om chloorgas (CL2) te vormen, die vervolgens uit de oplossing wordt vrijgegeven.
Samenvattend: Chloorgas vormt zich bij de positieve elektrode omdat chloride -ionen worden geoxideerd bij de anode, elektronen verliezen en chlooratomen vormen die combineren om chloorgas te vormen.
 Pre-Columbus klimaatverandering heeft mogelijk geleid tot afname van de Amazone-bevolking
Pre-Columbus klimaatverandering heeft mogelijk geleid tot afname van de Amazone-bevolking Wat is het doel van een lander?
Wat is het doel van een lander?  De positie en baan van de aarde leidden tot het uitsterven van het oude zeeleven
De positie en baan van de aarde leidden tot het uitsterven van het oude zeeleven NASA-wetenschapper verzamelt stukjes van het zonnestelsel van een Antarctische gletsjer
NASA-wetenschapper verzamelt stukjes van het zonnestelsel van een Antarctische gletsjer 180 miljoen jaar oude rotsen geven inzicht in de krachtigste aardbevingen op aarde
180 miljoen jaar oude rotsen geven inzicht in de krachtigste aardbevingen op aarde
Hoofdlijnen
- Welk micoorganisme wordt verspreid door de release van sporen?
- Wat gebeurde er met de ploidy aan het einde van de procesmitose?
- Wat is Tastile Stimulation?
- Klimaatverandering kan bamboe-lemuren langzaam uithongeren
- Welke moleculen in membraan geven hen hun specifieke functie beschrijven activiteiten van één deze moleculen?
- Wat is tamme gist?
- Wat is dat een goede wetenschapper?
- Wat beschouwen wetenschappers waarschijnlijk als belangrijk bewijs bij het classificeren van een onbekend organisme?
- De theorie verklaart waarom 25 procent van de culturen mannelijke geslachtsdelen afsnijdt
- Natuurkundigen werpen röntgenlicht op smeltende polymeren

- Eiwit afgeleid van haver is in nieuwe techniek gekoppeld aan celzelfmoord-enzym

- Onderzoekers ontdekken nieuwe strategie voor ontwikkeling van mensgeïntegreerde elektronica

- Natuurkundigen decoderen de dynamische interactie tussen moleculaire machines in metaal-organische raamwerken
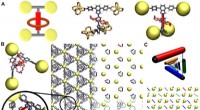
- Vloeibare metaalinkt maakt vorm vrij

 Hoe kunnen we de dichtheid van een onregelmatige vaste stof of vloeistof berekenen?
Hoe kunnen we de dichtheid van een onregelmatige vaste stof of vloeistof berekenen?  Wat is het belangrijkste metaal van roestvrij staal?
Wat is het belangrijkste metaal van roestvrij staal?  Auto-industrie problemen buffet Ford, Jaguar Landrover
Auto-industrie problemen buffet Ford, Jaguar Landrover Franse autogigant gaat assemblagefabriek opzetten in Namibië
Franse autogigant gaat assemblagefabriek opzetten in Namibië Nederlandse arrestatie man gekoppeld aan valutamixer Tornado Cash
Nederlandse arrestatie man gekoppeld aan valutamixer Tornado Cash Door zonne-energie aangedreven groene synthese van epoxiden
Door zonne-energie aangedreven groene synthese van epoxiden  Wat zijn de drie theorieën voor het ontstaan van Homo Sapiens?
Wat zijn de drie theorieën voor het ontstaan van Homo Sapiens?  Discriminatie op de woningmarkt staat succesvolle integratie in de weg
Discriminatie op de woningmarkt staat succesvolle integratie in de weg
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

