
Wetenschap
Welk gas laat brandend magnesium onmiddellijk uitgaan?
Het gas dat het brandende magnesium onmiddellijk maakt, is koolstofdioxide (CO2) .
Dit is waarom:
* magnesium is zeer reactief: Het brandt gemakkelijk in lucht en combineert met zuurstof om magnesiumoxide (MGO) te vormen.
* Koolstofdioxide is een brandonderdrukking: Het werkt als een deken, waardoor zuurstof het brandende magnesium bereikt.
* geen zuurstof, geen verbranding: Omdat het verbrandingsproces zuurstof vereist, stopt de afwezigheid van zuurstof de brandende reactie.
Belangrijke opmerking: Hoewel koolstofdioxide effectief is, moet u nooit proberen brandend magnesium met water te blussen. Water reageert gewelddadig met brandend magnesium, produceert brandbaar waterstofgas en veroorzaakt mogelijk een explosie.
 Welke voedingsstoffen zijn biologisch en of niet organisch?
Welke voedingsstoffen zijn biologisch en of niet organisch?  Wat zijn de elementen van KMnO4?
Wat zijn de elementen van KMnO4?  Welk onderscheidend symbool wordt gebruikt om radioactieve materialen te identificeren?
Welk onderscheidend symbool wordt gebruikt om radioactieve materialen te identificeren?  Welke symbolen zouden een chloorion vertegenwoordigen dat heeft geïoniseerd met stabiele elektronenconfiguratie A 35Cl1 B 35Cl2 C D 35CL?
Welke symbolen zouden een chloorion vertegenwoordigen dat heeft geïoniseerd met stabiele elektronenconfiguratie A 35Cl1 B 35Cl2 C D 35CL?  Wat is de naam van Compound S203?
Wat is de naam van Compound S203?
Hoofdlijnen
- Naamloze soorten bacteriën een naam geven in het tijdperk van big data
- Klonten als tijdelijke opslag
- Op welke vier manieren verschilt meiose van mitose?
- Organismen hebben over het algemeen veel genen die zich onafhankelijk bevatten dan het aantal van hun chromosomen waaraan dit fenomeen te wijten is?
- Wetenschappers ontcijferen hoe planten zonnebrand voorkomen
- Onderzoek suggereert dat gorilla's spontaan voedselreinigingsgedrag kunnen ontwikkelen
- Bloedsicles en baden houden Filippijnse dierentuindieren koel als de hittegolf toeslaat
- Oude genomen uit de Andes vertonen duidelijke aanpassingen aan landbouw en hoogte
- Wat zijn voordelen van eiwitten?
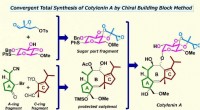
- Totale synthese van cotylenine A voor een nieuw geneesmiddel tegen kanker zonder bijwerkingen
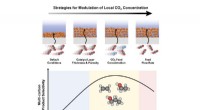
- Een nieuwe strategie voor de optimale elektroreductie van CO2 tot hoogwaardige producten
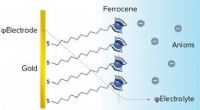
- Gecombineerde aanpak om grensvlakelektrochemie in meer detail te onderzoeken
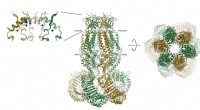
- Cellulaire klepstructuur opent potentiële nieuwe therapieën
- Olie opruimen met magneten
 Kan het deel van een bloem dat ei -cellen vasthoudt, de?
Kan het deel van een bloem dat ei -cellen vasthoudt, de?  Waarom is TE Mercator -projectiekaart nog steeds in gebruik vandaag?
Waarom is TE Mercator -projectiekaart nog steeds in gebruik vandaag?  Wat is de naam van acetylchloride IUPAC?
Wat is de naam van acetylchloride IUPAC?  Nieuw beeld van de ideale huisvrouw wordt gecreëerd door influencers en bloggers op sociale media
Nieuw beeld van de ideale huisvrouw wordt gecreëerd door influencers en bloggers op sociale media Studie vindt dat het veld van forensische antropologie diversiteit mist
Studie vindt dat het veld van forensische antropologie diversiteit mist Waarom beweegt de zon?
Waarom beweegt de zon?  Zijn bodems gevormd uit het gesteente genaamd resterende bodems?
Zijn bodems gevormd uit het gesteente genaamd resterende bodems?  Wat is .000000432 omgezet in wetenschappelijke notatie?
Wat is .000000432 omgezet in wetenschappelijke notatie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

