
Wetenschap
Wat is de gebalanceerde vergelijking die de reactie beschrijft tussen waterstofgas en stikstof om ammoniak NH3 te produceren?
n₂ + 3H₂ → 2NH₃
Hier is de uitsplitsing:
* n₂: Stikstofgas is een diatomee -molecuul, wat betekent dat het bestaat als twee stikstofatomen aan elkaar verbonden.
* 3H₂: Waterstofgas is ook diatomeeën, dus het bestaat als twee waterstofatomen aan elkaar zijn gebonden. We hebben drie moleculen H₂ nodig om de nodige waterstofatomen te bieden.
* 2NH₃: Het product, ammoniak, wordt gevormd met één stikstofatoom en drie waterstofatomen. We krijgen twee moleculen van NH₃ als gevolg van de reactie.
Deze vergelijking is in evenwicht omdat er gelijke getallen van elk type atoom zijn aan beide zijden van de vergelijking:
* stikstof: 2 aan beide kanten
* waterstof: 6 aan beide kanten
 Wanneer verandert een stof van vast naar vloeibaar?
Wanneer verandert een stof van vast naar vloeibaar?  Wat is molaire massa in de chemie?
Wat is molaire massa in de chemie?  Zwarte fosfor belooft de toekomst van elektronica
Zwarte fosfor belooft de toekomst van elektronica Hoeveel mol natriumhydroxide is nodig om 0,20 mol salpeterzuur te neutraliseren?
Hoeveel mol natriumhydroxide is nodig om 0,20 mol salpeterzuur te neutraliseren?  Waarom wordt kaliumpermanganaat verkleurd in aanwezigheid van 1-butanol 2-butanol maar langzaam verzendt door 2-methyl-2-propanol, hoewel alle drie alcoholen dezelfde moleculaire formule hebben?
Waarom wordt kaliumpermanganaat verkleurd in aanwezigheid van 1-butanol 2-butanol maar langzaam verzendt door 2-methyl-2-propanol, hoewel alle drie alcoholen dezelfde moleculaire formule hebben?
Hoofdlijnen
- Maagdelijke vrouwelijke spinnen gevonden bereid om zichzelf over te geven om levend te worden opgegeten door spinnetjes
- Waarom hebben meristematische cellen grote kernen?
- Tropische insecten zijn extreem gevoelig voor veranderende klimaten
- Wat is het deel van plantencel dat instructie bevat voor Called?
- Hoe vaak zijn er meerdere organismen geëvolueerd uit unicells?
- Is schimmels een gewervelde of ongewervelde dieren?
- Hoe gekoppelde gegevens en kunstmatige intelligentie dieren kunnen helpen
- Wat gebeurt er als we menselijke kwaliteiten toekennen aan bedrijven?
- Wat is de functie van fysiologie?
- Simulaties maken het mogelijk om stereochemie te kiezen voor je eigen avontuur

- Onderzoekers ontwikkelen extreem gevoelige waterstofsensor

- Collectieve ontvlechting van verstrengelde polymeren

- Composteerbaar bioleer biedt duurzame oplossingen voor de kledingindustrie en daarbuiten

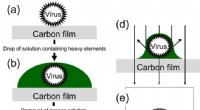
- Nieuw niet-radioactief, neutraal reagens onthult virussen in duidelijke details
 Welk symbool wordt gebruikt om verandering van snelheid te tonen?
Welk symbool wordt gebruikt om verandering van snelheid te tonen?  Welke instelling op een ijzer is 300 graden?
Welke instelling op een ijzer is 300 graden?  Een boek van 5 kg valt uit een plank. Als het landt met snelheid van 5,7 ms welke hoogte is gevallen?
Een boek van 5 kg valt uit een plank. Als het landt met snelheid van 5,7 ms welke hoogte is gevallen?  Wat eten schildpadden?
Wat eten schildpadden?  Satellietbeelden onthullen dat de aarde meer bossen heeft dan eerder werd gedacht
Satellietbeelden onthullen dat de aarde meer bossen heeft dan eerder werd gedacht  Wat zijn vier manieren waarop een kracht op een object kan handelen?
Wat zijn vier manieren waarop een kracht op een object kan handelen?  Duizenden boeren in Central Valley verliezen mogelijk toegang tot oppervlaktewater door toenemende droogte
Duizenden boeren in Central Valley verliezen mogelijk toegang tot oppervlaktewater door toenemende droogte Wat zijn drie kenmerken van duurzaam ecosysteem?
Wat zijn drie kenmerken van duurzaam ecosysteem?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

