
Wetenschap
Waarom verplaatst chloor de broom van kaliumbromide -oplossing?
* Elektrochemische serie: Chloor is hoger in de elektrochemische serie dan broom. Dit betekent dat chloor een sterkere neiging heeft om elektronen te winnen en negatieve ionen (anionen) te vormen.
* Reactiemechanisme: Wanneer chloorgas door een kaliumbromide -oplossing wordt geborreld, vindt de volgende reactie plaats:
`` `
CL2 (G) + 2KBR (AQ) → 2KCL (AQ) + BR2 (L)
`` `
* verplaatsing: Chlooratomen zijn meer reactief en accepteren gemakkelijk elektronen uit bromide-ionen (Br-), die chloride-ionen vormen (Cl-). Dit laat de broomatomen aan elkaar binden en vormen vloeibare broom (BR2), die wordt waargenomen als een roodbruine kleur in de oplossing.
in eenvoudiger termen: Chloor is een "sterker" niet-metaal dan broom en "wil" de elektronen meer. Dus het "steelt" het de elektronen uit broom en dwingt het uit de kaliumbromide -oplossing.
 Kunnen we zien dat het licht wordt uitgezonden door waterstofatomen wanneer ze overgaan op een grondtoestand?
Kunnen we zien dat het licht wordt uitgezonden door waterstofatomen wanneer ze overgaan op een grondtoestand?  Welke groep behoren zuurstofstikstof en zwavel?
Welke groep behoren zuurstofstikstof en zwavel?  Waarom elektron vrij in een metaal?
Waarom elektron vrij in een metaal?  Hoe scheiden je gewone zout- en zwavelpoeder?
Hoe scheiden je gewone zout- en zwavelpoeder?  Vraag ons is de vergelijking voor ethylalcohol met azijnzuur en con. zwavelzuur?
Vraag ons is de vergelijking voor ethylalcohol met azijnzuur en con. zwavelzuur?
 Nieuwe kaart van dagelijkse lichtintegralen gegenereerd op basis van bijgewerkte gegevens
Nieuwe kaart van dagelijkse lichtintegralen gegenereerd op basis van bijgewerkte gegevens Acht landen zijn nu uitgerust om de beschaving te beëindigen
Acht landen zijn nu uitgerust om de beschaving te beëindigen Onderzoek naar de vermindering van de steenkooluitstoot en de sterfte in China
Onderzoek naar de vermindering van de steenkooluitstoot en de sterfte in China  De richtlijnen voor drinkwater in de VS verschillen sterk van staat tot staat
De richtlijnen voor drinkwater in de VS verschillen sterk van staat tot staat Negrigreen-gletsjer in beweging
Negrigreen-gletsjer in beweging
Hoofdlijnen
- Gespecialiseerde cellen: definitie, soorten en voorbeelden
- Wat voor soort venatie heeft de Petunia -fabriek?
- Hoe cellen delen en zich voortplanten?
- Welke 2 processen worden gebruikt om macromoleculen en voedseldeeltjes door het celmembraan te verplaatsen?
- Nieuw onderzoek laat zien hoe meer boeren kunnen worden betrokken bij het ontwerpen van nieuw milieubeleid
- Zal het wegglijden of vastgrijpen:Wetenschappers vragen zich af:'Wat is slakkenslijm?'
- Waarom stoppen mensen dingen in categorieën?
- Wat zijn enkele soorten menselijke cellen?
- Bepaalde bacteriën produceren een chemische stof die hen resistent maakt tegen penicilline, aangezien deze zich aseksueel reproduceren, ze meestal nakomelingen?
- Onderzoekers onderzoeken structurele veranderingen in snel ingevroren eiwitten
- Zeesponzen blijven zitten met ankers die buigen maar niet breken

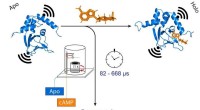
- Nieuwe SERS-strategie ontwikkeld voor bepaling van bèta-galactosidase-activiteit
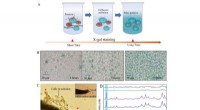
- Onderzoek naar de dynamiek van de vorming van nanodeeltjes uit een voorloper met atomaire resolutie

- Kleine chemische reactoren met microdruppels zorgen voor een revolutie in wetenschappelijke experimenten

 Hoe werken hydrodynamica?
Hoe werken hydrodynamica?  Wat is het momentum van een object van 20 kg?
Wat is het momentum van een object van 20 kg?  Wat betekent het hele aarde?
Wat betekent het hele aarde?  Homemade Math Games
Homemade Math Games  DNA toont aan dat de eerste moderne Brit een donkere huid had, blauwe ogen
DNA toont aan dat de eerste moderne Brit een donkere huid had, blauwe ogen Wat is de frequentie van een electomagnetische golf?
Wat is de frequentie van een electomagnetische golf?  Aan een waarnemer op een schip op zee welke breedtegraad verschijnt North Star het dichtst bij de horizon?
Aan een waarnemer op een schip op zee welke breedtegraad verschijnt North Star het dichtst bij de horizon?  Wat is een algemene observatie?
Wat is een algemene observatie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

