
Wetenschap
Hoeveel gram natriumcarbonaat bevatten 1.773 x 1017 koolstofatomen?
1. Vind de mol koolstofatomen:
* Het nummer van Avogadro vertelt ons dat er 6.022 x 10^23 atomen in één mol zijn.
* Verdeel het aantal koolstofatomen door het nummer van Avogadro om de mol koolstof te vinden:
(1.773 x 10^17 atomen) / (6.022 x 10^23 atomen / mol) =2,94 x 10^-7 mol C
2. Vind de mol natriumcarbonaat (NA2CO3):
* De formule voor natriumcarbonaat laat zien dat er één koolstofatoom per molecuul natriumcarbonaat is.
* Omdat het aantal mol koolstof en natriumcarbonaat in dit geval gelijk is, hebben we 2,94 x 10^-7 mol NA2CO3.
3. Bereken de massa natriumcarbonaat:
* Vind de molaire massa natriumcarbonaat:
* NA:22,99 g/mol (x2 =45,98 g/mol)
* C:12.01 g/mol
* O:16.00 g/mol (x3 =48,00 g/mol)
* Totale molaire massa:45,98 + 12.01 + 48,00 =105,99 g/mol
* Vermenigvuldig het mol natriumcarbonaat door zijn molaire massa:
(2.94 x 10^-7 mol) x (105,99 g/mol) = 3.12 x 10^-5 g Na2co3
Daarom bevatten 3.12 x 10^-5 gram natriumcarbonaat 1.773 x 10^17 koolstofatomen.
 Meer dan 400 doden door aardbeving in grensgebied tussen Iran en Irak (update)
Meer dan 400 doden door aardbeving in grensgebied tussen Iran en Irak (update) Wat maakt een goede boom? We gebruikten AI om vogels te vragen
Wat maakt een goede boom? We gebruikten AI om vogels te vragen  Hawaiis Kilauea-vulkaan stopt met uitbarsten na maandenlange lava
Hawaiis Kilauea-vulkaan stopt met uitbarsten na maandenlange lava NASA ziet tropische cycloon Irondro een oog ontwikkelen
NASA ziet tropische cycloon Irondro een oog ontwikkelen De geboorte en dood van een tektonische plaat
De geboorte en dood van een tektonische plaat
Hoofdlijnen
- Wanneer een levende plantencel water verliest door osmose, treedt er samentrekking van de inhoud op, weg van de muur. Hoe heet dit fenomeen?
- Hebben planten een microbioom?
- Wat is de reden voor hemiparese?
- Infectieziekten:CTRL + ALT + Delete
- Heeft een hybride allel er maar één voor eigenschap?
- Hoeveel Valence-elektronen heeft natrium?
- Wie heeft de moderne evolutietheorie opgericht?
- Tussen geometrie en biologie:hoe waarom is het aantal soorten afhankelijk van het gebied?
- Wat zijn de voorbeelden van wetenschappelijke overtuigingen?
- Veilig printen met onzichtbare inkt op waterbasis

- De crunch houden in vetarme chips

- Onderzoekers ontdekken dat sommige cidermakers onnodige suiker toevoegen

- Natuurkunde versus astma

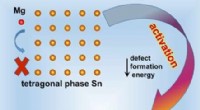
- Fasegrensregulering die de elektrochemische reactiviteit van op tin gebaseerde anodes voor magnesium-ionbatterijen stimuleert
 Hoe smartphones de planeet opwarmen
Hoe smartphones de planeet opwarmen Zonne-energiefeiten voor kinderen
Zonne-energiefeiten voor kinderen  Wetenschap zegt:bliksem zapt minder Amerikanen, niet meer
Wetenschap zegt:bliksem zapt minder Amerikanen, niet meer Expertpanel identificeert de belangrijkste klimaatrisico's voor Canada, aanpassingspotentieel
Expertpanel identificeert de belangrijkste klimaatrisico's voor Canada, aanpassingspotentieel Zijn de buitenste planeten 5 het verst van de zon?
Zijn de buitenste planeten 5 het verst van de zon?  Klimaatverandering gekoppeld aan meer bloemrijke bossen, studie toont
Klimaatverandering gekoppeld aan meer bloemrijke bossen, studie toont Het spotten van de eigen evolutie van kwantumtrucs van de natuur kan de kwantumtechnologie transformeren
Het spotten van de eigen evolutie van kwantumtrucs van de natuur kan de kwantumtechnologie transformeren Wat voor soort straling straalt een warmtelamp uit?
Wat voor soort straling straalt een warmtelamp uit?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

