
Wetenschap
Wat voor soort reactie is ammoniumnitraat en natriumhydroxide?
Dit is waarom:
* ammoniumnitraat (NH₄NO₃) is een zout gevormd uit een zwakke basis (ammoniak, NH₃) en een sterk zuur (salpeterzuur, HNO₃). In oplossing brengt het ammoniumionen (NH₄⁺) en nitraationen (NO₃⁻) uit.
* Natriumhydroxide (NaOH) is een sterke basis, het vrijgeven van natriumionen (Na⁺) en hydroxide -ionen (OH⁻) in oplossing.
De reactie:
NH₄NO₃ (aq) + NaOH (aq) → nH₃ (aq) + h₂o (l) + nano₃ (aq)
In deze reactie:
* Ammoniumionen (NH₄⁺) reageren met hydroxide -ionen (OH⁻) om ammoniak (NH₃) en water (H₂o) te vormen. Dit is de klassieke zuur-base neutralisatiereactie.
* Natriumionen (Na⁺) en nitraationen (NO₃⁻) blijven in oplossing als toeschouwersionen, niet direct betrokken bij de hoofdreactie.
Sleutelpunten:
* De reactie is exotherme , wat betekent dat het warmte vrijgeeft.
* De geproduceerde ammoniak is een zwakke basis, dus de oplossing zal na de reactie enigszins basic zijn.
* Deze reactie wordt vaak gebruikt om ammoniak in het laboratorium voor te bereiden.
 Hoeveel atomen zitten er in 3Cu(NO3)2?
Hoeveel atomen zitten er in 3Cu(NO3)2?  Een monster van 50 ml van een oplossing van 1,00 ml cuso4 wordt gemengd met 2 m koh in een calorimeter. De temperatuur van beide oplossingen was 20,2 C vóór het mengen en 26,3 °C na het mengen?
Een monster van 50 ml van een oplossing van 1,00 ml cuso4 wordt gemengd met 2 m koh in een calorimeter. De temperatuur van beide oplossingen was 20,2 C vóór het mengen en 26,3 °C na het mengen?  Wat is de dichtheid van grafeenoxide of grafeen?
Wat is de dichtheid van grafeenoxide of grafeen?  Dynamisch 3D-printproces met lichtgestuurde draai
Dynamisch 3D-printproces met lichtgestuurde draai Bij gebruik van papierchromatografie om schermmethyloranje te scheiden en welke beweegt het verste op papier?
Bij gebruik van papierchromatografie om schermmethyloranje te scheiden en welke beweegt het verste op papier?
 Waarom is moeilijk om te weten wat in de aarde eruit ziet?
Waarom is moeilijk om te weten wat in de aarde eruit ziet?  Recordniveaus van vrijgekomen kwik door ontdooiende permafrost in het Canadese Noordpoolgebied
Recordniveaus van vrijgekomen kwik door ontdooiende permafrost in het Canadese Noordpoolgebied Programma dat Lake Champlain bestudeert, komt in aanmerking voor maximaal $ 1 miljoen
Programma dat Lake Champlain bestudeert, komt in aanmerking voor maximaal $ 1 miljoen Desinvestering van fossiele brandstoffen zal de CO2-uitstoot verhogen, niet verlagen
Desinvestering van fossiele brandstoffen zal de CO2-uitstoot verhogen, niet verlagen Gefossiliseerde schelpen vertonen tekenen van verzuring van de oceaan vóór dinosaurusvernietigende asteroïde
Gefossiliseerde schelpen vertonen tekenen van verzuring van de oceaan vóór dinosaurusvernietigende asteroïde
Hoofdlijnen
- Het Nederlandse landschap verliest door insecten bestoven planten, zo blijkt uit 87 jaar data
- Wat beschrijft nauwkeurig hoe temperatuur de enzymactiviteit beïnvloedt?
- Waarom zou een wetenschapper de wetenschappelijke theorie afwijzen?
- Wat zijn de 2 dingen die nodig zijn om evolutie te laten plaatsvinden?
- Minder herkauwen, meer vergroening van de brandstof
- Uit onderzoek blijkt hoe cellen ‘vuilniszakken’ vormen voor het recyclen van afval
- Veldonderzoek heeft tot doel de verspreiding van door teken overgedragen ziekten in het Midwesten te vertragen
- Hoe weten cellen wanneer ze de celcyclus moeten doorlopen? Nieuwe studie vindt verband tussen verdeeldheid en groeisnelheid
- Hoe een moleculaire schakelaar de groei van plantenorganen vormgeeft
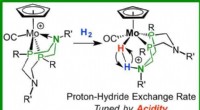
- Wetenschappers bepalen de snelheid van het breken en fixeren van diwaterstofmoleculen
- Radioactieve wolk boven Europa had civiele achtergrond

- Nieuwe moleculaire sondes voor opioïde receptoren

- Metalen nanokatalysatoren imiteren de structuur van enzymen

- Kunstmatige cellen reageren op veranderingen in de omgeving
 Waarom overtreden biologische organismen de wetten van de thermodynamica?
Waarom overtreden biologische organismen de wetten van de thermodynamica?  De genocide van gebarentalen:bescherming van de taalrechten van dove kinderen in Afrika
De genocide van gebarentalen:bescherming van de taalrechten van dove kinderen in Afrika Wat is glucose en waarom het belangrijk is?
Wat is glucose en waarom het belangrijk is?  Onderzoekers ontwikkelen door thermische straling regelbaar epsilon-bijna-nul-materiaal dat bestand is tegen extreme omgevingen
Onderzoekers ontwikkelen door thermische straling regelbaar epsilon-bijna-nul-materiaal dat bestand is tegen extreme omgevingen  Experts pleiten voor extra aandacht voor de impact van gletsjermassaverlies op stroomafwaartse systemen
Experts pleiten voor extra aandacht voor de impact van gletsjermassaverlies op stroomafwaartse systemen Wat gebeurt er met sedimenten tijdens depositie?
Wat gebeurt er met sedimenten tijdens depositie?  Vulkaanuitbarstingen op verschillende breedtegraden hebben een verschillende invloed op de temperatuur van het zeeoppervlak
Vulkaanuitbarstingen op verschillende breedtegraden hebben een verschillende invloed op de temperatuur van het zeeoppervlak Wordt de totale energie toeneemt wanneer de ene vorm van wordt omgezet in een andere vorm?
Wordt de totale energie toeneemt wanneer de ene vorm van wordt omgezet in een andere vorm?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

