
Wetenschap
Is zuurstof elektronegatiefer dan zwavel?
Dit is waarom:
* elektronegativiteit is de neiging van een atoom om elektronen naar zichzelf aan te trekken in een chemische binding.
* zuurstof heeft een hogere elektronegativiteitswaarde (3,44) dan zwavel (2.58) Op de schaal van Pauling.
* Dit komt omdat zuurstof kleiner is dan zwavel, wat betekent dat de valentie -elektronen dichter bij de kern zijn en een sterkere aantrekkingskracht ervaren.
* Bovendien heeft zuurstof een grotere nucleaire lading (meer protonen) dan zwavel, waardoor de trekkracht van elektronen verder wordt vergroot.
Als gevolg hiervan zal zuurstof in een binding tussen zuurstof en zwavel de neiging hebben om de gedeelde elektronen sterker aan te trekken, waardoor de binding polair is.
 Nieuw bewijs onthult de bron van Sanriku uit 1586, Japanse tsunami
Nieuw bewijs onthult de bron van Sanriku uit 1586, Japanse tsunami Nieuwe studie onthult dat sterke El Nino-gebeurtenissen grote veranderingen in Antarctische ijsplaten veroorzaken
Nieuwe studie onthult dat sterke El Nino-gebeurtenissen grote veranderingen in Antarctische ijsplaten veroorzaken Wetenschappers onderzoeken hoe verschillende huizen en levensstijlen van invloed zijn op welke insecten bij ons leven
Wetenschappers onderzoeken hoe verschillende huizen en levensstijlen van invloed zijn op welke insecten bij ons leven  COVID-19 en andere pandemieën zijn de effecten van onze negatieve impact op de diversiteit van het totale milieu
COVID-19 en andere pandemieën zijn de effecten van onze negatieve impact op de diversiteit van het totale milieu Waarom politiek het slechtste in ons naar boven haalt
Waarom politiek het slechtste in ons naar boven haalt
Hoofdlijnen
- Wat is een oplossing in de wetenschap?
- Welk deel van de plant maakt suiker?
- Hoe verschilt cauka's van primair?
- Het nepnieuwsprobleem van Facebook:wat is de verantwoordelijkheid ervan?
- Waarom zou Wegener een interdisciplinaire wetenschapper kunnen worden genoemd?
- Hoe globalisering menselijke parasieten virulenter kan maken
- Kun je biologie in een zin gebruiken?
- In beweging blijven - platte wormen werpen licht op de rol van migrerende stamcellen bij kanker
- Hoeveel soorten biomen zijn er?
- Het toepassen van computationele chemie om realistische chemische processen te simuleren

- Moleculaire simulaties laten zien hoe medicijnen belangrijke receptoren blokkeren

- Kinderen houden niet van bloemkool, broccoli kan in hun microbioom worden geschreven

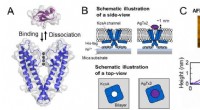
- Mechanisme van remming van schorpioentoxine van K+-kanaal opgehelderd met behulp van snelle AFM
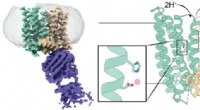
- Onthulling van de onverwachte structuur van ijzer-exporteur ferroportine
 Nanotechnologie en zonlicht maken de weg vrij voor een betere zichtbaarheid
Nanotechnologie en zonlicht maken de weg vrij voor een betere zichtbaarheid De nadelen van Smelter
De nadelen van Smelter Waarom kunnen we door de voormalige berg in Canada rijden zonder stijgende hoogte?
Waarom kunnen we door de voormalige berg in Canada rijden zonder stijgende hoogte?  Welke soorten stoffen zijn pure materie?
Welke soorten stoffen zijn pure materie?  Aardbeienvelden voor altijd? De productie leidt tot langdurige plasticvervuiling, zo blijkt uit onderzoek
Aardbeienvelden voor altijd? De productie leidt tot langdurige plasticvervuiling, zo blijkt uit onderzoek  Waar zijn de aardezon en maan tijdens een zonsverduistering?
Waar zijn de aardezon en maan tijdens een zonsverduistering?  Beschrijf twee manieren waarop wetenschappers de leeftijd van het universum berekenen?
Beschrijf twee manieren waarop wetenschappers de leeftijd van het universum berekenen?  Hoe vormen Mountain Breezes en Valley?
Hoe vormen Mountain Breezes en Valley?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

