
Wetenschap
Hoe globalisering menselijke parasieten virulenter kan maken
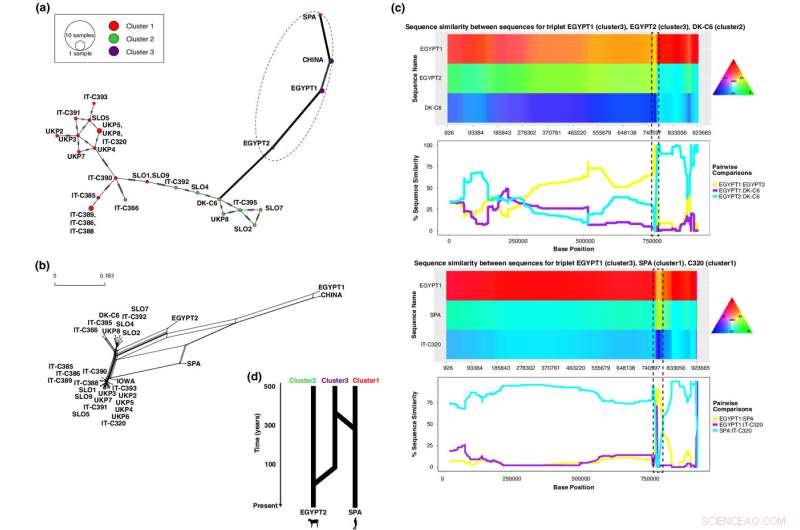
Recombinatie-analyse van chromosoom 1 identificeert twee hybride sequenties, Spa1 (een menselijk isolaat uit cluster 1) en Egypt 2 (een kalverisolaat uit cluster 3). (a) Netwerk dat aantoont dat haplotypes van hybride isolaten Spa1 en Egypt2 afwijken van de rest van de isolaten en nauw verbonden zijn met hun minder belangrijke oudersequenties (cluster 3-isolaten). (b) Fylogenetisch netwerk dat lussen toont tussen hybride isolaten, die potentiële recombinatie vertegenwoordigen. (c) Sequentieovereenkomstgrafieken verkregen met HybridCheck voor verschillende tripletten van isolaten die betrokken zijn bij een recombinatiegebeurtenis (hybride, hoofdouder, minderjarige ouder). De sequentieovereenkomst wordt weergegeven langs chromosomale posities (x-as) door een kleurenkaart waarin regio's met hetzelfde polymorfisme kleuren delen (boven) en door lijngrafieken die de procentuele overeenkomst op de y-as (onder) aangeven. Grafieken van recombinante regio's die een grote overeenkomst vertonen tussen hybride isolaten en hun minder belangrijke oudersequenties in de recombinante regio's zijn ingesloten in gestippelde vakken. (d) Schematische weergave van recombinatiegebeurtenissen in hybride isolaten, waaruit blijkt dat Egypt2 en Spa1 beide genetische variatie ontvingen van een cluster 3, ongeveer 49 (21-96; 95% BI) en 289 (204-395; 95% BI) jaar geleden, respectievelijk. Krediet:Moleculaire ecologie (2022). DOI:10.1111/mec.16556
Volgens nieuw onderzoek van de Universiteit van East Anglia worden parasieten die ernstige diarree veroorzaken waarschijnlijk virulenter vanwege de snelheid waarmee ze hun DNA uitwisselen en evolueren.
Onderzoekers bestudeerden de genomen van Cryptosporidium parvum, een zoönotische parasiet die ernstige diarree veroorzaakt bij zowel mens als dier.
Ze ontdekten dat verschillende geslachten van deze parasieten in toenemende mate hun DNA uitwisselen, waardoor de parasiet sneller is geëvolueerd, wat mogelijk kan resulteren in meer virulente en beter aangepaste stammen.
De nieuwe studie toont aan dat de Cryptosporidium parvum-lijnen de afgelopen 200 jaar meer DNA hebben uitgewisseld dan in de hele tijd daarvoor.
En ze schrijven dit toe aan globalisering en ons steeds nauwer contact met dieren, waardoor het aantal overloopgebeurtenissen toeneemt.
Een van de hoofdonderzoekers, Prof. Cock Van Oosterhout, van de UEA's School of Environmental Sciences, zei:"Cryptosporidium is een belangrijk geslacht van zoönotische parasieten en het is een van de vele micro-organismen die diarree veroorzaken bij zowel mensen als sommige dieren. In mensen, is het verantwoordelijk voor ongeveer 57.000 sterfgevallen per jaar, waarvan 80% onder kinderen jonger dan vijf jaar.
"De overgrote meerderheid hiervan bevindt zich in lage-inkomenslanden, maar uitbraken komen ook voor in het VK en elders in Europa. Er is geen effectief medicijn of vaccin beschikbaar, dus het is van cruciaal belang om de overdracht en evolutie van deze parasiet te begrijpen.
"We weten dat er verschillende lijnen zijn van de Cryptosporidium parvum-parasiet, maar we wilden meer weten over hoe ze evolueren, en vooral waarom deze soort mogelijk virulenter wordt dan in het verleden."
Het team, geleid door UEA in samenwerking met wetenschappers in Italië en Australië, maakte gebruik van volledige genoomsequentie-analyse om meer te weten te komen over deze genetische uitwisselingen.
Ze vergeleken 32 volledige genoomsequenties van menselijke en dierlijke stammen die zijn verzameld in Europa, de VS, Egypte en China.
Prof. Van Oosterhout zei:"We ontdekten dat verschillende geslachten van deze parasieten in toenemende mate hun DNA uitwisselen. In de afgelopen 200 jaar is ongeveer 22 procent van het genoom van deze parasieten uitgewisseld.
"Dit is aanzienlijk meer dan het DNA dat ze al die tijd eerder hebben uitgewisseld. De genen die betrokken zijn bij virulentie lijken in het bijzonder te worden beïnvloed door dergelijke genetische uitwisselingen. Het genoom van parasieten die mensen infecteren, bezit enig DNA van parasieten die normaal in koeien en lam.
"Wij geloven dat deze genetische uitwisselingen de parasiet helpen sneller te evolueren, en dat dit kan resulteren in meer virulente en beter aangepaste menselijke parasieten. Dit is erg belangrijk omdat, zoals COVID-19 ons heeft laten zien, menselijke parasieten snel kunnen evolueren.
"We veronderstellen dat de evolutiesnelheid verder wordt versneld omdat de parasiet kan evolueren in meerdere gastheersoorten. Dit betekent dat nieuwe aanpassingen die zijn geëvolueerd in parasieten die één gastheersoort infecteren, nu kunnen worden gebruikt door parasieten die een andere soort gastheren infecteren.
"De toegenomen connectiviteit in onze geglobaliseerde wereld en het nauwe contact tussen mensen en gedomesticeerde dieren verhoogt de snelheid van spill-over en spillback-gebeurtenissen.
"Met behulp van volledige genoomsequentieanalyse kunnen we deze genetische uitwisselingen nu bestuderen en identificeren wanneer en waar ze plaatsvinden. Dit zal ons helpen deze opkomende infectieziekten van zoönotische parasieten en pathogenen beter onder controle te houden," voegde hij eraan toe.
"Recente genetische uitwisselingen en vermenging vormen het genoom en de populatiestructuur van een zoönotische parasiet" is gepubliceerd in het tijdschrift Molecular Ecology .
 Nieuwe materialen om branden in lithium-ionbatterijen te helpen stoppen, explosies en de prestaties van de batterij verbeteren
Nieuwe materialen om branden in lithium-ionbatterijen te helpen stoppen, explosies en de prestaties van de batterij verbeteren Bioprinted aderen onthullen nieuwe details over medicijndiffusie
Bioprinted aderen onthullen nieuwe details over medicijndiffusie Wetenschappers pionieren met het maken van programmeerbare kunstmatige weefsels van synthetische cellen
Wetenschappers pionieren met het maken van programmeerbare kunstmatige weefsels van synthetische cellen Hoe Borax te converteren naar boorzuur
Hoe Borax te converteren naar boorzuur  High School Biology Experiment Ideas
High School Biology Experiment Ideas
 3D digitaal stadsmodel analyseert effecten van het blokkeren van zonlicht
3D digitaal stadsmodel analyseert effecten van het blokkeren van zonlicht Een blik op hoe het veranderende klimaat de gebouwenvoorraad in de staat New York beïnvloedt
Een blik op hoe het veranderende klimaat de gebouwenvoorraad in de staat New York beïnvloedt Studie hervormt het begrip van de impact van klimaatveranderingen op vroege samenlevingen
Studie hervormt het begrip van de impact van klimaatveranderingen op vroege samenlevingen Model koppelt patronen in sediment aan regen, stijging en zeespiegelverandering
Model koppelt patronen in sediment aan regen, stijging en zeespiegelverandering Corps of Engineers overweegt overstromingsbeheer op basis van de natuur
Corps of Engineers overweegt overstromingsbeheer op basis van de natuur
Hoofdlijnen
- Stages of Mitosis (Cell Division)
- Onverwachte bevinding in de energiecentrale van cellen
- Blade runner benen geven verminkte Thaise hond nieuw leven
- Eenvoudige manieren om de structuren van de Skull
- Onderzoekers vinden dat er minstens 14, 003 plantensoorten in het Amazonebekken
- Pangolin-handel dwingt Ghana om naar nieuwe natuurwetten te kijken
- Stille mutaties helpen bacteriën antibiotica te ontwijken
- Foster-kikkervisjes triggeren het ouderlijk instinct bij gifkikkers
- Het verschil tussen hoe interne en externe regulatoren werken
- Wat hebben we geleerd van het Human Genome Project?
- Onderzoek naar plantenenzymen toont aan dat eiwitten hun structurele rangschikking met verrassend gemak kunnen veranderen
- Hoe is het schrijven geëvolueerd?
- Analyse van oud DNA onthult een voorheen niet-herkend geslacht van uitgestorven paarden dat ooit door Noord-Amerika zwierf

- Onderzoekers vinden dat er minstens 14, 003 plantensoorten in het Amazonebekken

 Snellere colloïdale fluorescentiestralers:Nanoplatelets
Snellere colloïdale fluorescentiestralers:Nanoplatelets Facebook weet al anderhalf jaar dat Instagram slecht is voor tieners, ondanks dat het anders beweert
Facebook weet al anderhalf jaar dat Instagram slecht is voor tieners, ondanks dat het anders beweert Een in, twee uit:Efficiëntere zonnecellen simuleren
Een in, twee uit:Efficiëntere zonnecellen simuleren Dramatische toename van microplastics in zeegrasbodem sinds de jaren 70
Dramatische toename van microplastics in zeegrasbodem sinds de jaren 70 NASA test parachutesysteem voor landend ruimtevaartuig op Mars
NASA test parachutesysteem voor landend ruimtevaartuig op Mars Bazen met stemmingswisselingen maken werknemers het meest angstig
Bazen met stemmingswisselingen maken werknemers het meest angstig Het verschil tussen atomen, ionen, moleculen en verbindingen
Het verschil tussen atomen, ionen, moleculen en verbindingen  Nuke-opslagplaats in New Mexico onderzocht voor opslag van plutonium
Nuke-opslagplaats in New Mexico onderzocht voor opslag van plutonium
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

