
Wetenschap
Hoeveel elektronen verliezen fluor bij het vormen van een ion?
Fluorine zal niet Verlies elektronen bij het vormen van een ion. Het zal eigenlijk wonen Eén elektron.
Dit is waarom:
* Fluor's Electron Configuration: Fluor heeft 9 elektronen, met de configuratie 2, 7. Dit betekent dat het 7 elektronen in de buitenste schaal (valentieschaal) heeft.
* octetregel: Atomen hebben de neiging elektronen te winnen of te verliezen om een stabiele configuratie te bereiken met 8 elektronen in hun buitenste schaal. Dit staat bekend als de Octet -regel.
* een elektron winnen: Fluor kan een stabiel octet bereiken door één elektron te winnen, wat resulteert in een negatieve lading (-1). Dit creëert het fluoride-ion (F-).
Daarom krijgt fluor één elektron om een fluoride -ion te worden.
 Wat zijn de namen van 3 elementen die vaste stoffen in hun natuurlijke staat?
Wat zijn de namen van 3 elementen die vaste stoffen in hun natuurlijke staat?  Verbetering van de productie van waterstofperoxide door duurzame fotokatalyse
Verbetering van de productie van waterstofperoxide door duurzame fotokatalyse Welke formule toont het aantal en de soorten atomen in een molecuul, maar niet de bindingen?
Welke formule toont het aantal en de soorten atomen in een molecuul, maar niet de bindingen?  Wat is een afvalproduct van de ademhaling?
Wat is een afvalproduct van de ademhaling?  Waar of niet waar, de temperatuur van een stof verandert tijdens een toestandsverandering?
Waar of niet waar, de temperatuur van een stof verandert tijdens een toestandsverandering?
Hoofdlijnen
- Kunnen genen ons liberaal of conservatief maken?
- Wat is de naam van nucleotiden heeft geen DNA en RNA?
- Hoe diepe hersenstimulatie werkt
- De studie van de biologie omvat dingen die ooit leefden en degenen die vandaag in leven waren, waar of onwaar?
- Kunnen data dolfijnen redden? Hoe wetenschappers NASA-gegevens gebruiken om het verband tussen zonnestormen en het stranden van dieren te bestuderen
- Genen die alleen worden gezien in combinatie met een recessief gen?
- Wat zijn objecten die trillende oorzaakr -luchtmoleculen?
- Wat motiveert de verkoop van bestuivervriendelijke planten?
- Wat heeft een celmembraan dat het voor bepaalde moleculen gemakkelijker maakt om het membraan over te steken?
- Nieuwe schaal voor elektronegativiteit herschrijft het leerboek scheikunde

- Katalyseren van de omzetting van biomassa naar biobrandstof
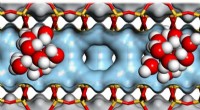
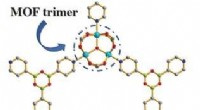
- Sterk resorptieve metaal-organische raamwerken
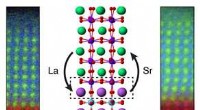
- Het benutten van verloren atomen kan helpen bij het maken van nieuwe, nooit eerder vertoonde oxiden
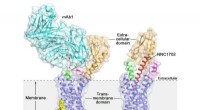
- Glucagon-receptorstructuur biedt nieuwe mogelijkheden voor het ontdekken van geneesmiddelen voor type 2 diabetes
 De zwaartekracht aan een kind uitleggen
De zwaartekracht aan een kind uitleggen Hoe is het genoom als een open boek? Nieuw onderzoek toont het ‘bibliotheeksysteem’ van cellen aan
Hoe is het genoom als een open boek? Nieuw onderzoek toont het ‘bibliotheeksysteem’ van cellen aan  Waarom vallen alle lichamen met dezelfde versnelling in afwezigheid van luchtwrijving?
Waarom vallen alle lichamen met dezelfde versnelling in afwezigheid van luchtwrijving?  Oppervlaktemeren zorgen ervoor dat Antarctische ijsplaten buigen
Oppervlaktemeren zorgen ervoor dat Antarctische ijsplaten buigen Waarom is er zo weinig wind op de locaties waar de cellen van de atmosfeercirculatie samenkomen?
Waarom is er zo weinig wind op de locaties waar de cellen van de atmosfeercirculatie samenkomen?  Autonoom Waymo-voertuig betrokken bij ongeval met 5 auto's in Arizona
Autonoom Waymo-voertuig betrokken bij ongeval met 5 auto's in Arizona Waar stort een ster in als zijn elementen sterft?
Waar stort een ster in als zijn elementen sterft?  Hoeveel jagen is te jagen?
Hoeveel jagen is te jagen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

