
Wetenschap
Welke groep metalen wordt gekenmerkt door een enkele valentie -elektron en zijn zeer reactieve atomen?
De groep metalen gekenmerkt door een enkele valentie -elektron en zijn zeer reactieve atomen de alkali -metalen .
Dit is waarom:
* Elektron met één valentie: Alkali -metalen hebben slechts één elektron in hun buitenste schaal, waardoor ze zeer enthousiast zijn om dit elektron te verliezen en een stabiele, volledige buitenste shell -configuratie te bereiken.
* Hoge reactiviteit: Deze neiging om een elektron te verliezen maakt ze zeer reactief. Ze reageren gemakkelijk met water, zuurstof en andere niet -metalen om ionische verbindingen te vormen.
Voorbeelden van alkali -metalen zijn onder meer:
* Lithium (li)
* Natrium (NA)
* Kalium (k)
* Rubidium (RB)
* Cesium (CS)
* Francium (fr)
Hoofdlijnen
- Plantensporen worden rechtstreeks geproduceerd door?
- Noem de 4 cellen die door oögenese worden geproduceerd?
- Cryo-EM-beeldvorming suggereert hoe de dubbele helix zich scheidt tijdens replicatie
- Geheugenhack:doe wat aerobics vier uur na de les
- Wat is de rol RNA tijdens vertaling?
- Was het geheime kruid in oergenensoep een verdikkingsmiddel?
- Hoe wordt het interne membraansysteem voor chloroplast genoemd?
- Hoe zijn zowel een bewerkingen als een gevolgtrekking hoe ze verschillen?
- Primaire en secundaire seksuele kenmerken
- Eenvoudige methode voor op keramiek gebaseerde flexibele elektrolytplaten voor lithium-metaalbatterijen

- Onderzoekers ontwikkelen nieuwe heterostructuurkatalysator voor effectieve waterstofproductie door watersplitsing

- Wetenschappers maken bioplastic voor voedselverpakkingen dat in twee jaar wordt afgebroken

- Kleurveranderende verbanden detecteren en behandelen bacteriële infecties

- Chaperones bereiden eiwitten gewoon voor om zelf te vouwen
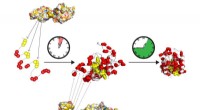
 Speciale levering:Macromoleculen via spinnenbeet
Speciale levering:Macromoleculen via spinnenbeet Wanneer wind eroderen alleen fijnkorrelig sediment dat grove sedimenten achterlaat?
Wanneer wind eroderen alleen fijnkorrelig sediment dat grove sedimenten achterlaat?  Hoe is de positie van Noord -Amerika ten opzichte van de evenaar de afgelopen 200 miljoen jaar veranderd?
Hoe is de positie van Noord -Amerika ten opzichte van de evenaar de afgelopen 200 miljoen jaar veranderd?  Wat is een drone?
Wat is een drone?  Hoeveel genen worden in de hoogte van de mens uitgenomen?
Hoeveel genen worden in de hoogte van de mens uitgenomen?  Waarom is kalksteen goed voor bodem?
Waarom is kalksteen goed voor bodem?  Hoe lelijke labels de aankoop van onaantrekkelijke producten kunnen verhogen
Hoe lelijke labels de aankoop van onaantrekkelijke producten kunnen verhogen Wall Street begroet bitcoin met interesse en zorgen
Wall Street begroet bitcoin met interesse en zorgen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


