
Wetenschap
Wat is de valentie van H2O?
Dit is waarom:
* waterstof (h): Elk waterstofatoom heeft een valentie van 1.
* zuurstof (O): Zuurstof heeft een valentie van 2.
In water deelt het zuurstofatoom zijn twee elektronen met twee waterstofatomen, waardoor twee covalente bindingen worden gevormd. Dit resulteert in een stabiel molecuul.
In plaats van "valentie" kunnen we praten over de "oxidatietoestanden" van de elementen in het watermolecuul:
* waterstof (h): +1
* zuurstof (O): -2
Dit geeft aan dat het zuurstofatoom een groter deel van de elektronen in de covalente bindingen "vasthoudt".
Dus, hoewel we niet praten over de "valentie" van H₂o, kunnen we de structuur en binding ervan begrijpen op basis van de valenties van de individuele atomen erin.
 Wat is de relatieve grootte van 3 subatomaire deeltjes?
Wat is de relatieve grootte van 3 subatomaire deeltjes?  Wat zijn niet-voorbeelden van geleiding?
Wat zijn niet-voorbeelden van geleiding?  Hoe zou uw antwoord op de molaire massa van CO2 veranderen als u voor gebruik niet zorgvuldig watervorst uit droogijs had geschraapt en druppels te klein waren om te zien in de kolf?
Hoe zou uw antwoord op de molaire massa van CO2 veranderen als u voor gebruik niet zorgvuldig watervorst uit droogijs had geschraapt en druppels te klein waren om te zien in de kolf?  Welk geluid reist het beste, hoewel vast vloeibaar gas?
Welk geluid reist het beste, hoewel vast vloeibaar gas?  Lichtgevoelige trigger ontwikkeld voor de geprogrammeerde celdeling en dood
Lichtgevoelige trigger ontwikkeld voor de geprogrammeerde celdeling en dood
 Diepe diamanten bevatten bewijs van recyclingprocessen in de diepe aarde
Diepe diamanten bevatten bewijs van recyclingprocessen in de diepe aarde Feiten over de Wooly Mammoth
Feiten over de Wooly Mammoth  Wat koude hagedissen in Miami ons kunnen vertellen over de veerkracht tegen klimaatverandering
Wat koude hagedissen in Miami ons kunnen vertellen over de veerkracht tegen klimaatverandering  Wat wordt bedoeld met lagere soortendiversiteit?
Wat wordt bedoeld met lagere soortendiversiteit?  Je groeide in een grot, maar je bent niet leeft begonnen met water en mineralen die nu solide de lucht nooit zien wat je?
Je groeide in een grot, maar je bent niet leeft begonnen met water en mineralen die nu solide de lucht nooit zien wat je?
Hoofdlijnen
- Wat bevat erfelijke informatie?
- Eiwitten zijn lange moleculen die zijn gebouwd uit welke verschillende combinaties?
- Amerikaanse biologische klok-genetici winnen Nobelprijs voor Geneeskunde 2017
- Wat maakt plantencelwanden zowel sterk als uitbreidbaar?
- Wat 'Big Data' onthult over de diversiteit aan soorten
- Wetenschappers laten zien hoe verschuivingen in temperatuur de immuunrespons bevorderen
- Virusstamping - een veelzijdige nieuwe methode voor genetische manipulatie van afzonderlijke cellen
- Het is misschien tijd om de houdbaarheidsdatum op voedselverpakkingen te schrappen, zeggen slimme verpakkingsonderzoekers
- Ambien
- Laten we de vloeistof-vloeistof-interface onder ogen zien

- Chemici maken harde kunststoffen recyclebaar

- Sterke kunstmatige spieren van koolstofvezel kunnen 12 optillen, 600 keer hun eigen gewicht

- Structuur van supercomplex van fotosysteemproteïne van diatomeeën onthult zijn zeer geavanceerde energieoverdrachtsnetwerk
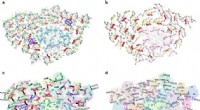
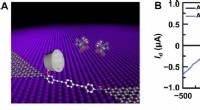
- Een elektrische benadering met één molecuul voor aminozuurdetectie en chiraliteitsherkenning
 China's koolstofdoelstelling brengt grote economieën in een radicale klimaatconsensus
China's koolstofdoelstelling brengt grote economieën in een radicale klimaatconsensus Hoe Concordes werken
Hoe Concordes werken  Angstige klanten gevoelig voor omvang en reikwijdte van een datalek, terwijl boze klanten dat niet zijn
Angstige klanten gevoelig voor omvang en reikwijdte van een datalek, terwijl boze klanten dat niet zijn Ook al heeft de zon een grotere massa dan aardmaan, omdat wat dan de zon is?
Ook al heeft de zon een grotere massa dan aardmaan, omdat wat dan de zon is?  De wereld treft 8 miljard mensen; Is dat goed of slecht?
De wereld treft 8 miljard mensen; Is dat goed of slecht?  Kun je mij een zin geven waarin het woord celmembraan wordt gebruikt?
Kun je mij een zin geven waarin het woord celmembraan wordt gebruikt?  Wat is het totaal van originele en nieuwe stoffen die hetzelfde zijn na een chemische verandering?
Wat is het totaal van originele en nieuwe stoffen die hetzelfde zijn na een chemische verandering?  Hoe het combineren van Inuit-kennis en westerse wetenschap de gezondheid van ijsberen kan helpen verbeteren
Hoe het combineren van Inuit-kennis en westerse wetenschap de gezondheid van ijsberen kan helpen verbeteren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

