
Wetenschap
Hoe zou uw antwoord op de molaire massa van CO2 veranderen als u voor gebruik niet zorgvuldig watervorst uit droogijs had geschraapt en druppels te klein waren om te zien in de kolf?
* waterverontreiniging: Water (H₂o) heeft een molaire massa van 18 g/mol, terwijl CO₂ een molaire massa van 44 g/mol heeft. De aanwezigheid van water in de kolf, zelfs in kleine druppeltjes, zou bijdragen aan de totale gemeten massa.
* Verhoogde massa, onveranderde mol: Omdat het water niet reageert met de co₂, blijft het aantal mol co₂ ongewijzigd. De totale massa neemt echter toe als gevolg van het toegevoegde water.
* Hogere berekende molaire massa: De molaire massa wordt berekend als massa/mol. Met een verhoogde massa en hetzelfde aantal mol, zou de berekende molaire massa hoger zijn dan de werkelijke molaire massa van CO₂.
Samenvattend: De aanwezigheid van waterdruppeltjes zou leiden tot een overschatting van de co₂ molaire massa omdat de massa die in de berekening wordt gebruikt, zou worden opgeblazen.
 Ontdek hoe cocaïne werkt
Ontdek hoe cocaïne werkt  Wetenschappers analyseren structuur, mechanisme van faageiwit dat elektronen steelt
Wetenschappers analyseren structuur, mechanisme van faageiwit dat elektronen steelt Wanneer conc h2so4 op de vloer terechtkomt, kan het worden gereinigd door?
Wanneer conc h2so4 op de vloer terechtkomt, kan het worden gereinigd door?  Nieuws duurzaam plantaardig plastic ter ondersteuning van orgaanonderzoek
Nieuws duurzaam plantaardig plastic ter ondersteuning van orgaanonderzoek Neemt de oplosbaarheid toe naarmate de temperatuur toeneemt?
Neemt de oplosbaarheid toe naarmate de temperatuur toeneemt?
 Onderzoekers suggereren dat rampen met kolenas en residudammen kunnen worden voorkomen
Onderzoekers suggereren dat rampen met kolenas en residudammen kunnen worden voorkomen Het verlies aan biodiversiteit heeft gevolgen voor samenlevingen en economieën:hoe kan Europa de verspreiding van invasieve soorten het hoofd bieden?
Het verlies aan biodiversiteit heeft gevolgen voor samenlevingen en economieën:hoe kan Europa de verspreiding van invasieve soorten het hoofd bieden?  Tropical Rain Forest Biome Landscape Kenmerken
Tropical Rain Forest Biome Landscape Kenmerken  Overstromingswater zorgt voor gifstoffen uit rivierbeddingen
Overstromingswater zorgt voor gifstoffen uit rivierbeddingen Satellieten volgen de voedselvoorziening van de naties
Satellieten volgen de voedselvoorziening van de naties
Hoofdlijnen
- Waarom moet je weten dat biologie een dierenarts is?
- Wat is abstract zelfstandig naamwoord van verdamping?
- Wat is de natuurlijke omgeving van dierencel?
- Hoe menselijke transportgewoonten het gedrag van kleine mijten helpen verklaren
- Tijdens glycolyse wordt ATP geproduceerd hoeveel netto moleculen worden gevormd?
- Onderzoek naar diversiteit in celdeling:Studie onderzoekt het evolutieproces dat diverse levenscycli ondersteunt
- Onderzoeker onthult hoe kevers terugveren van bosbranden
- Het kwantumfysica-concept van kritische massa
- Hoe reproduceert Acinetobacter Baumannii?
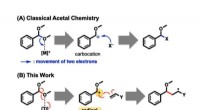
- Radicale chemie maakt eenvoudige synthese van ethers mogelijk
- Hoogwaardige elektrokatalysatoren om de ontwikkeling van directe ethanolbrandstofcellen te stimuleren

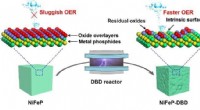
- Etsproces verbetert de extractie van waterstof tijdens elektrolyse van water
- Onderzoekers ontwerpen een verbeterde route naar koolstofneutrale kunststoffen

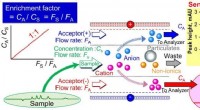
- Verbetering van de gevoeligheid voor analyse van ionische opgeloste stoffen
 Heb je het gezien? Supermoon siert de hemel over de hele wereld
Heb je het gezien? Supermoon siert de hemel over de hele wereld  Studie onderzoekt hoe risicotolerantie verandert rond betaaldag
Studie onderzoekt hoe risicotolerantie verandert rond betaaldag  Wat is de naam van formule CR3P2?
Wat is de naam van formule CR3P2?  Wat betekent halfzon en maan?
Wat betekent halfzon en maan?  Waar staat -4800 om in wetenschappelijke notatie?
Waar staat -4800 om in wetenschappelijke notatie?  Hoge beloften voor autonome auto's onvervuld
Hoge beloften voor autonome auto's onvervuld Resolutie van een hoek het universum?
Resolutie van een hoek het universum?  Manipuleren van de draairichting van kunstmatige moleculaire motoren met behulp van supramoleculen
Manipuleren van de draairichting van kunstmatige moleculaire motoren met behulp van supramoleculen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

