
Wetenschap
Vriestpunt is de op welke vloeistof verandert in vaste, welk effect kan het vriespunt veranderen?
factoren die het vriespunt beïnvloeden:
* Druk:
* Over het algemeen: Verhogende druk meestal * verhoogt * het vriespunt. Dit komt omdat druk de dichtere toestand (vaste) bevordert over de minder dichte toestand (vloeistof).
* Water is een uitzondering: Water is ongebruikelijk. Toenemende druk op vloeibaar water daadwerkelijk * verlaagt * het vriespunt. Dit komt omdat ijs minder dicht is dan water, dus druk is de vloeibare toestand begunstigt.
* onzuiverheden:
* Opgeloste opgeloste stoffen: Het toevoegen van onzuiverheden (zoals zout, suiker of andere opgeloste stoffen) aan een vloeistof * verlaagt * het vriespunt. Dit staat bekend als de depressie van het vriespunt. Hoe meer onzuiverheden, hoe groter de depressie.
* Opgehangendeeltjes: De aanwezigheid van gesuspendeerde deeltjes (zoals vuil of zand) kan een klein effect hebben op het vriespunt, maar het is meestal minder significant dan opgeloste onzuiverheden.
* intermoleculaire krachten:
* Sterkere krachten: Vloeistoffen met sterkere intermoleculaire krachten (zoals waterstofbinding) hebben de neiging om * hogere * vriespunten te hebben. Dit komt omdat er meer energie nodig is om de sterke attracties tussen moleculen uit elkaar te breken om een vaste stof te vormen.
* zwakkere krachten: Vloeistoffen met zwakkere intermoleculaire krachten (zoals van der Waals -krachten) hebben * lagere * vriespunten.
* Moleculaire structuur:
* De grootte, vorm en symmetrie van moleculen kunnen beïnvloeden hoe ze samen in een vaste stof inpakken. Dit kan het vriespunt beïnvloeden, waardoor het hoger of lager is, afhankelijk van de specifieke structuur.
Voorbeeld:
Laten we eens kijken naar water:
* Puur water: Bevriest bij 0 ° C (32 ° F) bij standaard atmosferische druk.
* zout water: De toevoeging van zout (NaCl) verlaagt het vriespunt onder 0 ° C. Daarom gebruiken we zout om ijs te smelten op wegen in de winter.
Samenvattend:
Het vriespunt van een vloeistof is een complexe eigenschap die wordt beïnvloed door factoren zoals druk, onzuiverheden, intermoleculaire krachten en moleculaire structuur. Door deze factoren te begrijpen, kunnen we vriespunten voorspellen en manipuleren voor verschillende toepassingen.
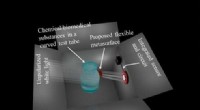
 Chemici creëren een moleculaire emissiethermometer
Chemici creëren een moleculaire emissiethermometer  Waar of niet waar is chemische energie een soort potentieel dat te wijten is aan de samenstelling van de stof?
Waar of niet waar is chemische energie een soort potentieel dat te wijten is aan de samenstelling van de stof?  Geleidt zwavel elektriciteit in waterige oplossing?
Geleidt zwavel elektriciteit in waterige oplossing?  Wat is de chemische formule van natriumbifosfaat?
Wat is de chemische formule van natriumbifosfaat?  Wat is beter oplosbaar bariumhydroxide of kaliumhydroxide?
Wat is beter oplosbaar bariumhydroxide of kaliumhydroxide?
 Kun je een perzikboom met pruimenboom bestuiven?
Kun je een perzikboom met pruimenboom bestuiven?  Eén graad opwarming van de aarde veroorzaakt een 50% toename van het risico op ontheemding
Eén graad opwarming van de aarde veroorzaakt een 50% toename van het risico op ontheemding Earths 2019 resources budget uitgegeven tegen 29 juli:rapport
Earths 2019 resources budget uitgegeven tegen 29 juli:rapport NASA vindt overblijfselen van Nardas die regen naar Mexico brengen, op weg naar het zuidwesten van de VS
NASA vindt overblijfselen van Nardas die regen naar Mexico brengen, op weg naar het zuidwesten van de VS Om de klimaatcrisis aan te pakken hebben we meer democratie nodig, niet minder
Om de klimaatcrisis aan te pakken hebben we meer democratie nodig, niet minder
Hoofdlijnen
- Hoe lang bekende genen onderzoekers blijven verrassen
- Chimpansees kunnen leren gereedschap te gebruiken zonder anderen te observeren
- Kan rijst water uit landbouwvelden filteren?
- Waarom hebben bacteriën geen kern?
- Gefixeerd op eten?
- Het mysterie,
- Kan gezichtsblindheid verklaren waarom die persoon op het werk mij nooit gedag zegt?
- Welke suiker componeert een deel van het ATP -molecuul?
- Nieuwe technologie zal laten zien hoe RNA de genactiviteit reguleert
- Katoen maken dat brandveilig en comfortabel is

- Organische zonnecellen die 10 jaar meegaan in de ruimte

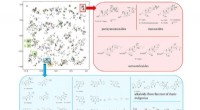
- SMART:gezichtsherkenning voor moleculaire structuren
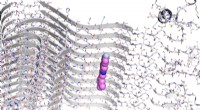
- Onderzoekers ontdekken nieuwe moleculen voor het volgen van de ziekte van Parkinson
- Een metaholografisch platform dat blootstelling aan licht detecteert
 Vermont verlaagt prikkels voor programma voor hernieuwbare energie
Vermont verlaagt prikkels voor programma voor hernieuwbare energie Wat is een homogene mengsel van twee of meer pure stoffen die worden genoemd?
Wat is een homogene mengsel van twee of meer pure stoffen die worden genoemd?  Het bestaan van een magnetisch veld van meer dan 3,5 miljard jaar geleden staat nog steeds ter discussie
Het bestaan van een magnetisch veld van meer dan 3,5 miljard jaar geleden staat nog steeds ter discussie Rapport:De rol van op geloof gebaseerde organisaties bij het reageren op moderne slavernij
Rapport:De rol van op geloof gebaseerde organisaties bij het reageren op moderne slavernij Welk element smelt bij de lagere temperatuur-zuurstof of kwik?
Welk element smelt bij de lagere temperatuur-zuurstof of kwik?  Epic Games breekt durfkapitaalrecords in een topjaar voor bedrijven in North Carolina
Epic Games breekt durfkapitaalrecords in een topjaar voor bedrijven in North Carolina Milky Way vs Andromeda (omdat ze nu kans maakten)
Milky Way vs Andromeda (omdat ze nu kans maakten) Een gas bij dezelfde temperatuur als vloeibare toestand?
Een gas bij dezelfde temperatuur als vloeibare toestand?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

