
Wetenschap
Solid natriumhydroxide ontleedt zich in gasvormig water en vaste oxide?
Ontleding van natriumhydroxide
Natriumhydroxide (NaOH) ontleedt bij verwarming, maar de producten zijn:
* natriumoxide (Na₂o) , een vaste stof
* waterstofgas (H₂) , een gas
De reactie:
2 NaOH (S) → Na₂o (S) + H₂ (G)
Verklaring:
* De sterke ionische bindingen in NaOH breken wanneer verwarmd, waardoor de natrium- en hydroxide -ionen worden vrijgeeft.
* Waterstofionen (H⁺) van de hydroxide -ionen combineren om waterstofgas te vormen (H₂).
* Natriumionen (Na⁺) combineren met resterende oxide -ionen (o²⁻) om natriumoxide (Na₂o) te vormen.
Belangrijke opmerking:
De ontleding van natriumhydroxide vereist dat zeer hoge temperaturen (boven 500 ° C) effectief optreden. Bij lagere temperaturen blijft NaOH stabiel.
Laat het me weten als je nog andere chemische vragen hebt!
 Wat gebeurt er als je olie aan water en vervolgens emulgator toevoegt en schudt?
Wat gebeurt er als je olie aan water en vervolgens emulgator toevoegt en schudt?  Zijn er vier koolstof- en waterstofatomen in CH4?
Zijn er vier koolstof- en waterstofatomen in CH4?  Waarom heeft het dinatriumzout van EDTA de voorkeur boven EDTA?
Waarom heeft het dinatriumzout van EDTA de voorkeur boven EDTA?  Afvalkooldioxide gebruiken om metalen van ertsen te scheiden
Afvalkooldioxide gebruiken om metalen van ertsen te scheiden Wat is de algemene naam voor koolstoftetrahydride en waarvoor werd het gebruikt?
Wat is de algemene naam voor koolstoftetrahydride en waarvoor werd het gebruikt?
 Smog moet stoppen met spelen, Indiase artsen vertellen cricketbazen
Smog moet stoppen met spelen, Indiase artsen vertellen cricketbazen Wat was hot vóór 1976? Een reis door Britse weersomstandigheden memory lane
Wat was hot vóór 1976? Een reis door Britse weersomstandigheden memory lane Afvalwaterbehandeling voor een derde van de grootte en kosten
Afvalwaterbehandeling voor een derde van de grootte en kosten Ze hebben het bos voor altijd beheerd. Daarom zijn ze van cruciaal belang in de strijd tegen de klimaatverandering
Ze hebben het bos voor altijd beheerd. Daarom zijn ze van cruciaal belang in de strijd tegen de klimaatverandering  Wetenschappers gebruiken oren in de grond om de ogen van orkanen te volgen
Wetenschappers gebruiken oren in de grond om de ogen van orkanen te volgen
Hoofdlijnen
- Wat wordt gemaakt door organisme met de genotype TTSS?
- Wat is zoetwaterbiota?
- Hoe worden dinosaurusweefsels diep in de tijd bewaard?
- Zijn de dochtercellen identiek of genetisch verschillend?
- De positieve kant van een besmettelijk eiwit:stresssensoren bevorderen de overleving van gistcellen
- Wat zijn de belangrijkste functies van Cilia & Flagella?
- Hoe eiwitreceptoren op cellen in- en uitschakelen
- Waarom je moet letten op vliegend braaksel
- Welke gebieden in het DNA bevatten herhaalde segmenten?
- Goedkoop, schaalbare watersplitsing voedt de toekomstige waterstofeconomie

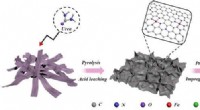
- Wetenschappers stellen nieuwe bifunctionele katalysatoren voor op van biomassa afgeleide koolstof
- Infraroodsensor dient als een nieuw hulpmiddel voor het ontdekken van medicijnen

- Elektronenversnellers onthullen de radicale geheimen van antioxidanten

- Wetenschappers ontwikkelen een effectief systeem voor de levering van biomateriaal aan laboratoria

 TED-gesprekken proberen optimisme te injecteren in pandemische somberheid
TED-gesprekken proberen optimisme te injecteren in pandemische somberheid Wetenschappers ontwikkelen NIF-optiek van de volgende generatie om energie te verhogen en schade te beperken
Wetenschappers ontwikkelen NIF-optiek van de volgende generatie om energie te verhogen en schade te beperken Ingenieurs bedenken een niet-invasieve techniek om het gezichtsvermogen te corrigeren
Ingenieurs bedenken een niet-invasieve techniek om het gezichtsvermogen te corrigeren NASA's Juno om Jupiters maan Ganymedes van dichtbij te bekijken
NASA's Juno om Jupiters maan Ganymedes van dichtbij te bekijken Hoe is de manier waarop een mesa vergelijkbaar is met canyon -vormen?
Hoe is de manier waarop een mesa vergelijkbaar is met canyon -vormen?  Sandwichkatalysatoren bieden een hogere activiteit en duurzaamheid
Sandwichkatalysatoren bieden een hogere activiteit en duurzaamheid Wat is het woordvergelijking voor reactie tussen zilvernitraat en kaliumbromide?
Wat is het woordvergelijking voor reactie tussen zilvernitraat en kaliumbromide?  Breng kinderen in de echte wereld voor effectief bosbrandonderwijs
Breng kinderen in de echte wereld voor effectief bosbrandonderwijs
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

