
Wetenschap
Waarom heeft het dinatriumzout van EDTA de voorkeur boven EDTA?
Oplosbaarheid: Dinatrium-EDTA is beter oplosbaar in water dan EDTA. Dit komt omdat de natriumionen in het dinatriumzout helpen de waterstofbruggen tussen de EDTA-moleculen te verbreken, waardoor ze beter oplosbaar worden. De hogere oplosbaarheid van dinatrium-EDTA maakt de bereiding van oplossingen met een hogere concentratie mogelijk, wat voor bepaalde toepassingen voordelig kan zijn.
Stabiliteit: Dinatrium-EDTA is stabieler in oplossing dan EDTA. EDTA kan hydrolyse ondergaan in waterige oplossingen, wat leidt tot de vorming van metaalcomplexen en het vrijkomen van protonen. Dit kan de pH van de oplossing verlagen en de effectiviteit van EDTA als chelaatvormer verminderen. Het dinatriumzout van EDTA is minder gevoelig voor hydrolyse, wat betekent dat het zijn chelaatvormende eigenschappen over een breder bereik aan pH-waarden kan behouden.
pH: Dinatrium-EDTA heeft een hogere pH dan EDTA. Dit komt omdat de natriumionen in het dinatriumzout helpen de protonen te neutraliseren die vrijkomen door de EDTA-moleculen. De hogere pH van dinatrium-EDTA maakt het minder corrosief voor metalen oppervlakken en biologische weefsels. Dit kan een belangrijke overweging zijn bij toepassingen waarbij EDTA wordt gebruikt als reinigingsmiddel of bij medische procedures.
Over het geheel genomen maken de hogere oplosbaarheid, stabiliteit en pH van dinatrium-EDTA het voor veel toepassingen de voorkeurskeuze.
 Litouwen roept noodtoestand uit omdat boeren te maken krijgen met droogte
Litouwen roept noodtoestand uit omdat boeren te maken krijgen met droogte De aarde had de koelste februari ooit sinds 2014
De aarde had de koelste februari ooit sinds 2014 Het lokale bergklimaat wordt beïnvloed door de bladoppervlakteverhouding in de omliggende bossen
Het lokale bergklimaat wordt beïnvloed door de bladoppervlakteverhouding in de omliggende bossen Hoe wordt zuurstof uit onze waterwegen 'gezogen'?
Hoe wordt zuurstof uit onze waterwegen 'gezogen'?  Een diep reservoir van primordiaal helium in de aarde
Een diep reservoir van primordiaal helium in de aarde
Hoofdlijnen
- DNA van een Incajongen die 500 jaar geleden werd geofferd, laat zien hoe mensen zich naar Zuid-Amerika verspreidden
- Ziek dolfijnkalf verbetert met sondemelk, helpende handen
- Amerikaanse eiken delen een gemeenschappelijke noordelijke voorouder
- Wat is een Punnett-vierkant?
- Rapport:meer dan 1.000 wilde paarden naar de slachtbank gestuurd
- Dominant Allele: wat is het? & Waarom gebeurt het? "(with Traits Chart)
- Het ontwikkelen van een symbiotische relatie tussen E. coli en stinkwantsen onthult aanwijzingen over hoe symbiose zich ontwikkelt
- Hoe een dodelijke salmonellasoort zijn infectietactieken verfijnt
- MS-onderzoek:Myeline beïnvloedt hoe hersencellen signalen verzenden
- Een eenvoudige methode om vlakke microstructuren van polysiloxaan af te drukken
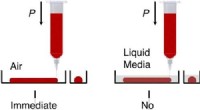
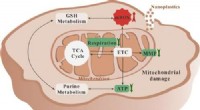
- Nanoplastics kunnen menselijke lever- en longcelprocessen verstoren in laboratoriumexperimenten
- Bronnen voor teambeeldvorming die worden gebruikt in internationale experimenten met nieuwe fotokatalysatoren
- Eenvoudig apparaat bewaakt de gezondheid met behulp van zweet

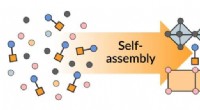
- Een eenvoudige manier om complexe halfgeleiders zichzelf te laten assembleren
 Wetenschappers stellen nieuwe bron voor zeldzame subatomaire deeltjes voor
Wetenschappers stellen nieuwe bron voor zeldzame subatomaire deeltjes voor Hoe steden de klimaatverandering het beste kunnen bestrijden
Hoe steden de klimaatverandering het beste kunnen bestrijden  Welke fysiologische aanpassing zou het transportproces in een plant verminderen?
Welke fysiologische aanpassing zou het transportproces in een plant verminderen?  Drie astronauten veilig aan boord van het internationale ruimtestation (update)
Drie astronauten veilig aan boord van het internationale ruimtestation (update) Kun je een ster doden met ijzer?
Kun je een ster doden met ijzer?  Experimenten tonen aan dat de gegevens over het vroege leven volledig 'vals-positieven' kunnen zijn
Experimenten tonen aan dat de gegevens over het vroege leven volledig 'vals-positieven' kunnen zijn  Van een raam naar een spiegel:nieuw materiaal maakt de weg vrij voor sneller computergebruik
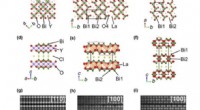
Van een raam naar een spiegel:nieuw materiaal maakt de weg vrij voor sneller computergebruik B-site op steenzout geordende Cu-gebaseerde dubbele perovskiet realiseert hoge efficiëntie en stabiele CO₂-elektroreductie
B-site op steenzout geordende Cu-gebaseerde dubbele perovskiet realiseert hoge efficiëntie en stabiele CO₂-elektroreductie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

