
Wetenschap
Hoeveel mol zuurstof in 30L gas?
Dit is waarom:
* De ideale gaswet: De relatie tussen volume, druk, temperatuur en mol van een gas wordt beschreven door de ideale gaswet:
* pv =nrt
* P: Druk (in atmosferen)
* v: Volume (in liters)
* n: Aantal mol
* r: Ideale gasconstante (0,0821 l · atm/mol · k)
* t: Temperatuur (in Kelvin)
* Oplossen voor mol (n): Om het aantal mol te vinden (N), herschikken we de vergelijking:
* n =pv / rt
Om de mol zuurstof in 30L gas te berekenen, moet u de druk en temperatuur geven.
Voorbeeld:
Laten we zeggen dat de druk 1 atm is en de temperatuur 25 ° C (298K) is.
1. Converteer de temperatuur naar Kelvin: 25 ° C + 273.15 =298.15 K
2. Sluit de waarden aan op de formule:
* n =(1 atm * 30 l) / (0.0821 l · atm / mol · k * 298.15 k)
* n ≈ 1,23 mol zuurstof
Daarom heeft u de druk en temperatuur nodig om het aantal mol zuurstof in 30L gas te bepalen.
 Nieuwe elektrokatalysatoren luiden koolstofneutraliteit in
Nieuwe elektrokatalysatoren luiden koolstofneutraliteit in Waarom is het mogelijk dat koolstof zoveel verschillende soorten verbindingen vormen?
Waarom is het mogelijk dat koolstof zoveel verschillende soorten verbindingen vormen?  Welke invloed heeft het type materiaal op de weerstand?
Welke invloed heeft het type materiaal op de weerstand?  Hoeveel mol zijn er in 6,5 gram zwavel S?
Hoeveel mol zijn er in 6,5 gram zwavel S?  Beoordeling van de impact van verliesmechanismen in zonnecelkandidaat-antimoonsulfideselenide
Beoordeling van de impact van verliesmechanismen in zonnecelkandidaat-antimoonsulfideselenide
 Het dumpen van giftig afval in de Golf van Guinee komt neer op milieuracisme
Het dumpen van giftig afval in de Golf van Guinee komt neer op milieuracisme Wat zijn herbivoren of carnivoren van zee -apen?
Wat zijn herbivoren of carnivoren van zee -apen?  Gesteentemonsters geven aan dat water een belangrijk ingrediënt is voor korstvorming
Gesteentemonsters geven aan dat water een belangrijk ingrediënt is voor korstvorming Satelliet trekt de aandacht van snel intensiverende tropische cycloon Cilida
Satelliet trekt de aandacht van snel intensiverende tropische cycloon Cilida Onderzoeker ontwikkelt nieuw model om historische aardbevingen nauwkeurig te dateren
Onderzoeker ontwikkelt nieuw model om historische aardbevingen nauwkeurig te dateren
Hoofdlijnen
- Welke twee van de volgende kenmerken moeten een hypothese bezitten om wetenschappelijk te zijn?
- Wat gebruikt 2 of meer lenzen om levende cellen te vergroten?
- Wat is verse embryo's?
- Waarom hebben plantencellen zowel celwanden als celmembranen?
- Hé voorstedelijke mensen, ontmoet de buren:tekendragende witstaarthert
- Hoe Risso's dolfijnen een evenwicht vinden tussen het inhouden van hun adem en het vinden van voedsel
- Wat zijn drie soorten planten die native zijn?
- Waar in de stamcel van een embryo staan instructies voor het opbouwen van een hart?
- Wat is de oorsprong en betekenis van naam?
- Wetenschappers ontdekken dat watermicrodruppels kunnen veranderen in waterstofperoxide wanneer ze condenseren op koude oppervlakken

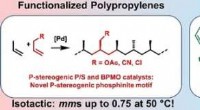
- Katalysatoren voor isotactische polaire polypropylenen
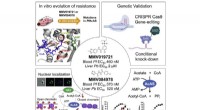
- Biologische ingenieurs vinden een nieuw doelwit voor malariamedicijnen
- Handige meting van de antioxidantcapaciteit van voedsel

- Synthetische chemie haalt antikankerverbindingen uit de zeeslak en het laboratorium in

 60 cm is gelijk aan thuis vele centimeter?
60 cm is gelijk aan thuis vele centimeter?  Wat is het volume van een gouden bar van 25 kg 24-karaats van 999,99 fijnheid?
Wat is het volume van een gouden bar van 25 kg 24-karaats van 999,99 fijnheid?  Kun je de maan op Antarctica zien?
Kun je de maan op Antarctica zien?  Identificatie van gemeenschappen die risico lopen op de gevolgen van extreme hitte
Identificatie van gemeenschappen die risico lopen op de gevolgen van extreme hitte COVID-19 verspilt veel Amerikaanse recyclingprogramma's
COVID-19 verspilt veel Amerikaanse recyclingprogramma's Op welke twee manieren kan de ouderrots het metamorfe proces beïnvloeden?
Op welke twee manieren kan de ouderrots het metamorfe proces beïnvloeden?  Berekening van ringkerntransformatoren
Berekening van ringkerntransformatoren Levenscyclus katoenstaart
Levenscyclus katoenstaart
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

