
Wetenschap
Is CH3BR een polair of niet -molecuul?
* elektronegativiteit: Bromine (BR) is aanzienlijk meer elektronegatief dan koolstof (C) en waterstof (H). Dit betekent dat Bromine elektronen sterker aantrekken in de C-BR-binding.
* Polaire covalente bindingen: De C-BR-binding is een polaire covalente binding, met een gedeeltelijke negatieve lading (8-) op het broomatoom en een gedeeltelijke positieve lading (Δ+) op het koolstofatoom.
* Moleculaire geometrie: Het molecuul heeft een tetraëdrische vorm. De polaire C-BR-binding creëert een dipoolmoment, dat een maat is voor de scheiding van lading in het molecuul. De andere C-H-obligaties hebben ook dipoolmomenten, maar ze zijn veel kleiner en annuleren elkaar.
* Algemeen dipoolmoment: Het totale dipoolmoment van het molecuul wijst naar het broomatoom.
Samenvattend resulteert de polaire C-BR-binding en de moleculaire geometrie in een netto dipoolmoment, waardoor CH3BR een polair molecuul is.
 Kunnen we het gat in de ozonlaag dichten?
Kunnen we het gat in de ozonlaag dichten?  Van kantoorramen tot Mars:wetenschappers debuteren superisolerende gel
Van kantoorramen tot Mars:wetenschappers debuteren superisolerende gel Hoe actief zijn de micro-organismen in jouw yoghurt? Chemici creëren een nieuw hulpmiddel om de probiotische activiteit te bestuderen
Hoe actief zijn de micro-organismen in jouw yoghurt? Chemici creëren een nieuw hulpmiddel om de probiotische activiteit te bestuderen  Computersimulaties geven inzicht in hoe koolstofdioxide reageert met een sekwestrerende vloeistof
Computersimulaties geven inzicht in hoe koolstofdioxide reageert met een sekwestrerende vloeistof  Wat is het verschil tussen perithecium en apothecium?
Wat is het verschil tussen perithecium en apothecium?
 Naarmate de warmte-index stijgt, spoedbezoeken, sterfgevallen stijgen in New England
Naarmate de warmte-index stijgt, spoedbezoeken, sterfgevallen stijgen in New England Wat bepaalt het klimaat van een gebied?
Wat bepaalt het klimaat van een gebied?  Onderzoekers vinden alarmerende NOx-uitstoot van dieselauto's
Onderzoekers vinden alarmerende NOx-uitstoot van dieselauto's Ingestorte gletsjers vergroten de onzekerheden op de derde pool:stroomafwaartse meren kunnen binnen tien jaar samenvloeien
Ingestorte gletsjers vergroten de onzekerheden op de derde pool:stroomafwaartse meren kunnen binnen tien jaar samenvloeien Brazilië registreert slechtste dag voor Amazon-branden in 15 jaar
Brazilië registreert slechtste dag voor Amazon-branden in 15 jaar
Hoofdlijnen
- Hoe wordt het genoemd als bacteriën zijn gastheer geen pijn doen?
- Waarom kunnen slangen niet knipperen?
- Is een hypothese de verklaring voor theorie?
- Wat voor soort cel functioneert meiose bij de vorming van?
- Wat is het nuttige micro -organisme dat aanwezig is in wrongel?
- Waarom ramon y Cajal neuronen de vlinder naar ziel genoemd?
- Verbetering van de kwaliteitsanalyse van zoete aardappel met hyperspectrale beeldvorming en AI
- Moleculaire biologieactiviteit stopt bij welke Temptaurure?
- Afrika zit vol met vleermuizen, maar hun fossielen zijn schaars – waarom deze zeldzame gegevens ertoe doen
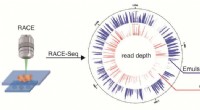
- Onderzoekers verbeteren de methode die het genoom koppelt aan functie voor eencellige omgevingscellen
- Nieuwe inzichten in vitamine A-recycling en zicht overdag

- Onderzoekers ontwikkelen een toxinevrij lijmsysteem geïnspireerd op onderwaterwezens

- Team ontwikkelt afscheider die gasovergang voor waterelektrolyse vermindert

- Knipper en je zult amyloïden niet missen

 Onderzoekers onthullen hoe mycorrhiza-soorten de koolstof in de plantenbodem in bossen reguleren
Onderzoekers onthullen hoe mycorrhiza-soorten de koolstof in de plantenbodem in bossen reguleren  Hoe maak je een ecosysteem met een schoenendoos
Hoe maak je een ecosysteem met een schoenendoos  De keerzijde van de Bitcoin:hoe blockchain duurzame energie kan ondersteunen
De keerzijde van de Bitcoin:hoe blockchain duurzame energie kan ondersteunen Onderzoek voorspelt hoe het eekhoornpokkenvirus zich zou kunnen verspreiden in grijze eekhoornpopulaties
Onderzoek voorspelt hoe het eekhoornpokkenvirus zich zou kunnen verspreiden in grijze eekhoornpopulaties  Welke formule relateert gewicht en massa?
Welke formule relateert gewicht en massa?  Welk organel in de plantencel maakt glucose uit zonlicht?
Welk organel in de plantencel maakt glucose uit zonlicht?  Betere batterijen door 3D chemische beeldvorming op nanoschaal
Betere batterijen door 3D chemische beeldvorming op nanoschaal Onderzoekers proberen mensachtig denken in machines na te bootsen
Onderzoekers proberen mensachtig denken in machines na te bootsen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

