
Wetenschap
Kan een vaste opgeloste stof worden opgelost in een waterige oplossing?
Dit is waarom:
* waterige oplossing: Dit betekent dat het oplosmiddel water is (h₂o).
* oplossen: Dit proces omvat de opgeloste deeltjes (vaste stof in dit geval) die van elkaar scheiden en omringd worden door oplosmiddelmoleculen (water).
Hoe het werkt:
1. Attractie: De watermoleculen hebben een polaire structuur (positieve en negatieve uiteinden). Ze worden aangetrokken door de opgeloste deeltjes, die polair of ionisch kunnen zijn.
2. ARGEMAKEN: De watermoleculen omringen de opgeloste deeltjes en trekken ze effectief weg van de vaste structuur.
3. Oplossing: Als de aantrekkelijke krachten tussen de watermoleculen en de opgeloste deeltjes sterker zijn dan de krachten die de opgeloste stof tegen elkaar houden, zal de vaste stof oplossen.
Voorbeelden:
* zout (NaCl) oplossen in water: De ionische bindingen in zout worden verbroken en de natrium (Na+) en chloride (Cl-) ionen worden omgeven door watermoleculen.
* suiker (c₁₂h₂₂o₁₁) oplossen in water: De polaire suikermoleculen vormen waterstofbruggen met watermoleculen en trekken ze in oplossing.
Belangrijke opmerking: Niet alle vaste stoffen lossen op in water. De oplosbaarheid van een vaste stof is afhankelijk van verschillende factoren, waaronder:
* Polariteit van de opgeloste stof: Polaire en ionische opgeloste stoffen zijn eerder opgelost in water.
* Temperatuur: Verhogende temperatuur verhoogt meestal de oplosbaarheid.
* Druk: Druk heeft een verwaarloosbaar effect op de oplosbaarheid van vaste stoffen in vloeistoffen.
 Wat is de atomaire massa van orthofosfairzuur?
Wat is de atomaire massa van orthofosfairzuur?  Onderzoekers ontdekken uniek materiaalontwerp voor hersenachtige berekeningen
Onderzoekers ontdekken uniek materiaalontwerp voor hersenachtige berekeningen Wat is het kookpunt voor Krypton om van een vloeibaar gas te draaien?
Wat is het kookpunt voor Krypton om van een vloeibaar gas te draaien?  Onderkoeld water is een stabiele vloeistof, zo laten wetenschappers voor het eerst zien
Onderkoeld water is een stabiele vloeistof, zo laten wetenschappers voor het eerst zien  Wetenschappers produceren robuuste katalysator om water in waterstof te splitsen zuurstof
Wetenschappers produceren robuuste katalysator om water in waterstof te splitsen zuurstof
 Rampen onder ogen:lessen van een eiland in Bangladesh
Rampen onder ogen:lessen van een eiland in Bangladesh Neutronenuitbarstingen van kosmische straling gebruiken om gammastraaluitbarstingen van bliksem te begrijpen
Neutronenuitbarstingen van kosmische straling gebruiken om gammastraaluitbarstingen van bliksem te begrijpen Anders omgaan met rampen is cruciaal voor kuststeden
Anders omgaan met rampen is cruciaal voor kuststeden Hoe hebben mensen invloed op Tasmanian Devil Habitats?
Hoe hebben mensen invloed op Tasmanian Devil Habitats?  Firefall-fenomeen verbaast bezoekers aan Yosemites El Capitan
Firefall-fenomeen verbaast bezoekers aan Yosemites El Capitan
Hoofdlijnen
- Afrikaanse gewassen bieden een voedzame, glutenvrije oplossing
- Waarom eet je in een lab?
- Uit een grootschalig onderzoek blijkt dat veel geplande wegen in de tropen niet gebouwd mogen worden
- Hoeveel sets van hetzelfde gen voor elk kenmerk ontvangen nakomelingen?
- Waarom zorgt de puberteit ervoor dat we stoppen met groeien?
- Kunnen genetisch gemodificeerde muggen malaria uitroeien?
- Studie vergelijkt Salmonella-percentages in monsters van commerciële pluimveehouderijen in de achtertuin
- Welke tool moet u gebruiken en groepsorganismen?
- Marine Protected Areas in Antarctica moeten jonge keizerspinguïns bevatten, zeggen wetenschappers
- Hoe kunnen onderzoekers snel toegang krijgen tot complexe moleculen voor het ontdekken van geneesmiddelen?

- Visualisatie van moleculaire beweging van gesubstitueerd 9-fosfaanthraceen

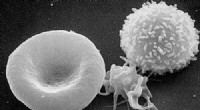
- Grote doorbraak in de productie van rode bloedcellen
- Het geheim van de behandeling van de achilleshiel van perovskiet-alternatieven voor siliciumzonnepanelen onthuld

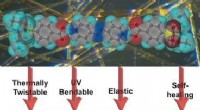
- Organische kristallen draaien, kromming, en genees
 Uitgaande Facebook-exec valt voor het inhuren van oppositiebedrijf
Uitgaande Facebook-exec valt voor het inhuren van oppositiebedrijf Onderzoekers creëren 3D-celarrays voor meer realistische experimentele biologische omgevingen
Onderzoekers creëren 3D-celarrays voor meer realistische experimentele biologische omgevingen Hulp nodig bij het bouwen van IKEA-meubels? Deze robot kan een handje helpen
Hulp nodig bij het bouwen van IKEA-meubels? Deze robot kan een handje helpen Wetenschappers klaar voor Cassini-missie naar de grote finale van Saturnus
Wetenschappers klaar voor Cassini-missie naar de grote finale van Saturnus oude gegevens, nieuwe trucs:nieuwe resultaten van NASA's Galileo-ruimtevaartuig 20 jaar later
oude gegevens, nieuwe trucs:nieuwe resultaten van NASA's Galileo-ruimtevaartuig 20 jaar later Transparantie van leiderschap alleen garandeert niet dat werknemers zich op de werkvloer zullen uitspreken
Transparantie van leiderschap alleen garandeert niet dat werknemers zich op de werkvloer zullen uitspreken  Verandering van de bodem de sleutel tot het verminderen van blootstelling aan lood bij kinderen
Verandering van de bodem de sleutel tot het verminderen van blootstelling aan lood bij kinderen Hoe wordt het weer beïnvloed door de Suns Energy?
Hoe wordt het weer beïnvloed door de Suns Energy?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

