
Wetenschap
Wat is volume O2 -gas in de ontleding 5,0 g HgO bij 550 graden Celsius A Druk 3 atm?
1. Evenwichtige chemische vergelijking:
De ontleding van kwik (II) oxide (HGO) wordt weergegeven door de volgende vergelijking:
2 HGO (S) → 2 Hg (L) + O₂ (G)
2. Mol HGO:
* Vind de molaire massa van HGO:
* HG:200,59 g/mol
* O:16.00 g/mol
* Molaire massa van HGO =200,59 + 16.00 =216,59 g/mol
* Bereken mol HGO:
* mol =massa / molaire massa
* mol =5,0 g / 216,59 g / mol =0,0231 mol hgo
3. Mol O₂:
* Gebruik de molverhouding van de gebalanceerde vergelijking:2 mol hgo produceren 1 mol o₂
* mol O₂ =(0,0231 mol HGO) * (1 mol O₂ / 2 mol HGO) =0,0116 mol O₂
4. Ideale gaswet:
* We zullen de ideale gaswet gebruiken om het volume van O₂ te vinden:
* Pv =nrt
* Waar:
* P =druk (in atm) =3 atm
* V =volume (in liters)
* n =mol gas =0,0116 mol
* R =ideale gasconstante =0,0821 l · atm/(mol · k)
* T =temperatuur (in kelvin) =550 ° C + 273.15 =823.15 k
5. Oplossen voor volume:
* V =(nrt) / p
* V =(0,0116 mol * 0,0821 l · atm / (mol · k) * 823.15 k) / 3 atm
* V ≈ 0,26 l
Daarom is het volume O₂ -gas geproduceerd uit de ontleding van 5,0 g HGO bij 550 ° C en 3 atm ongeveer 0,26 liter.
 Waarom zijn algaes beperkt tot water, terwijl varens land hebben aangepast?
Waarom zijn algaes beperkt tot water, terwijl varens land hebben aangepast?  Welke van deze wetenschappelijke disciplines registreert de vormen en locaties continenten?
Welke van deze wetenschappelijke disciplines registreert de vormen en locaties continenten?  Verontreinigende stoffen die al meer dan 30 jaar verboden zijn, blijven hangen in Britse rivieren - onze dieren in het wild zijn het bewijs
Verontreinigende stoffen die al meer dan 30 jaar verboden zijn, blijven hangen in Britse rivieren - onze dieren in het wild zijn het bewijs Kan de overgebleven warmte van de laatste El Nino een nieuwe brandstof opleveren?
Kan de overgebleven warmte van de laatste El Nino een nieuwe brandstof opleveren? Afbeelding:Calabrië, Italië, vanuit de ruimte
Afbeelding:Calabrië, Italië, vanuit de ruimte
Hoofdlijnen
- Hoe de hoed past:onderzoek naar structurele biologie onthult de vorm van het epigenetische enzymcomplex
- Welke kenmerken moet een levend ding worden geclassificeerd als een amfibie?
- Nieuw inzicht in hoe de oorzakelijke genproducten van xeroderma pigmentosum de nauwkeurigheid van DNA-reparatie garanderen
- Een vaccin voor eetbare planten? nieuwe gewasbeschermingsmethode in zicht
- Bavianengeslachten verschillen in de manier waarop sociale status 'onder de huid' komt
- Wat zit er in een naam? Big Data onthult onderscheidende patronen in hogeronderwijssystemen
- Een belangrijk buffersysteem in het menselijk lichaam is?
- De belangrijkste antigeenpresenterende cellen in het lichaam zijn?
- Welk dier begint met D moet carnivoren zijn?
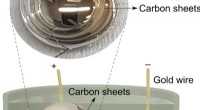
- Vloeibare metalen breken organische brandstoffen af tot ultradunne grafietplaten
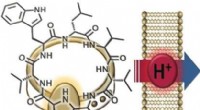
- Chemische synthese toont aan dat antibioticum uit de menselijke neus werkt door protontranslocatie
- Hoe gemeenschappelijke elementen een meer energiezekere toekomst kunnen maken

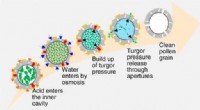
- Pollenschillen schoonmaken
- Metalen nanokatalysatoren imiteren de structuur van enzymen

 Welke moet gelden voor circumpolaire sterrenbeelden op de Zuidpool?
Welke moet gelden voor circumpolaire sterrenbeelden op de Zuidpool?  Kraakbeen kweken - geen gemakkelijke taak
Kraakbeen kweken - geen gemakkelijke taak Dit bedrijf wil afval delven om metalen voor EV-batterijen te vinden
Dit bedrijf wil afval delven om metalen voor EV-batterijen te vinden De beste zeoliet bouwen
De beste zeoliet bouwen Glimlachende menselijke gezichten zijn aantrekkelijk voor honden - dankzij oxytocine
Glimlachende menselijke gezichten zijn aantrekkelijk voor honden - dankzij oxytocine Kunstmatige intelligentie kan worden ingesteld om kantelpunten van klimaatverandering te onthullen
Kunstmatige intelligentie kan worden ingesteld om kantelpunten van klimaatverandering te onthullen Lost alcohol zout beter op dan water?
Lost alcohol zout beter op dan water?  Optische eigenschappen van polyethyleen
Optische eigenschappen van polyethyleen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

