
Wetenschap
Lost alcohol zout beter op dan water?
* polariteit: Water is een zeer polair molecuul, wat betekent dat het een positief en negatief einde heeft. Zout (NaCl) is ook een ionische verbinding met een positief (natrium) en negatief (chloride) uiteinde. Het positieve uiteinde van watermoleculen trekt de negatieve chloride -ionen aan en het negatieve uiteinde van watermoleculen trekt de positieve natriumionen aan. Met deze sterke aantrekkingskracht kan water de ionische bindingen in zout effectief uit elkaar breken en oplossen.
* Polariteit van alcohol: Hoewel alcohol ook polair is, is het minder polair dan water. Dit betekent dat de aantrekkingskracht tussen alcoholmoleculen en zoutionen zwakker is dan de aantrekkingskracht tussen watermoleculen en zoutionen. Als gevolg hiervan lost alcohol aanzienlijk minder zout op dan water.
Samenvattend: Water is een veel effectiever oplosmiddel voor zout vanwege de hogere polariteit en een sterkere aantrekkingskracht op de ionen in zout.
 Door vliegers geblazen Antarctische ontdekkingsreizigers maken de meest zuidelijke positie van Galileo vast
Door vliegers geblazen Antarctische ontdekkingsreizigers maken de meest zuidelijke positie van Galileo vast Is de houtkap echt gestopt in Victoria? Wat de dood van een met uitsterven bedreigd zweefvliegtuig ons vertelt
Is de houtkap echt gestopt in Victoria? Wat de dood van een met uitsterven bedreigd zweefvliegtuig ons vertelt  Zijn de vogels die uit de lucht vielen in Arkansas op nieuwe 2011 gekoppeld aan Falling Louisiana en Argentinië?
Zijn de vogels die uit de lucht vielen in Arkansas op nieuwe 2011 gekoppeld aan Falling Louisiana en Argentinië?  Indringende vraag:Wat is het verschil tussen kikkers en padden?
Indringende vraag:Wat is het verschil tussen kikkers en padden?  Te koop:uniek stuk grond in strategische Arctische archipel
Te koop:uniek stuk grond in strategische Arctische archipel
Hoofdlijnen
- Veel bacteriën kunnen zich niet reproduceren bij koelere temperaturen en worden hoog vernietigd. Hoe profiteren mensen van dit feit bij het bereiden van het opslaan van voedsel?
- Evolutie is vanzelfsprekend als een?
- Hoe hittegolven het Arctische fytoplankton beïnvloeden
- Wat zijn enkele obstakels voor sympatrische speciatie?
- Wat is predicetatie?
- Wat werkt onze hersenen samen om te creëren?
- Studie werpt nieuw licht op hoe dieren en planten reageren op veranderingen in de omgeving
- Glyfosaat:waar is het verboden of beperkt?
- Hoe een vormveranderende receptor de celgroei beïnvloedt
- Nieuw antibioticum verslaat bacteriële resistentie
- Potentieel voor een schoner brandstofmengsel

- Het creëren van lithium-ionbatterijen met een hogere energiedichtheid voor toepassingen op het gebied van hernieuwbare energie

- Laboratoriumtechnologie biedt duidelijkheid te midden van zorgen over waterverontreiniging in Hawaï

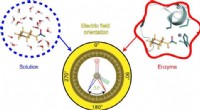
- Elektrische velden in kaart brengen om te helpen ontrafelen hoe enzymen werken
 Kleine moleculen, gigantisch (oppervlakte)potentieel
Kleine moleculen, gigantisch (oppervlakte)potentieel Paleontologen ontdekken nieuwe soorten sauropod-dinosaurussen in Tanzania
Paleontologen ontdekken nieuwe soorten sauropod-dinosaurussen in Tanzania Is een fosfaat-DNA of RNA?
Is een fosfaat-DNA of RNA?  Milieuvriendelijke lignine nanodeeltjes groenen zilveren nanobullet om bacteriën te bestrijden
Milieuvriendelijke lignine nanodeeltjes groenen zilveren nanobullet om bacteriën te bestrijden Exoplanet-missie krijgt ticket om te rijden
Exoplanet-missie krijgt ticket om te rijden Een groener proces voor het extraheren van verbindingen uit landbouw- en voedselafval
Een groener proces voor het extraheren van verbindingen uit landbouw- en voedselafval Het type suiker dat wordt gebruikt om schapenmelkkefir te zoeten, kan de acceptatie door de consument verbeteren
Het type suiker dat wordt gebruikt om schapenmelkkefir te zoeten, kan de acceptatie door de consument verbeteren Wat is het veiligste type nachtslot?
Wat is het veiligste type nachtslot?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

