
Wetenschap
Leg de regels uit die bepalen hoe elektronen zijn gerangschikt rond kernen van atomen?
De regels van elektronenarrangement:
De opstelling van elektronen rond de kern van een atoom wordt bepaald door een reeks regels op basis van kwantummechanica. Hier is een uitsplitsing:
1. Kwantumnummers:
* Hoofdkwantumnummer (n): Beschrijft het energieniveau van de elektron. Hogere 'n' betekent hogere energie. Het kan elk positief geheel getal zijn (1, 2, 3, ...), waarbij 1 de grondtoestand is.
* hoekmomentum of azimuthaal kwantumnummer (l): Beschrijft de vorm van het orbitaal van het elektron. Het varieert van 0 tot N-1.
* l =0:s orbital (sferisch)
* L =1:P Orbital (Dumbbell -vormig)
* l =2:D orbital (meer complexe vormen)
* l =3:f orbital (nog complexere vormen)
* magnetisch kwantumnummer (ml): Beschrijft de oriëntatie van het orbitaal in de ruimte. Het kan waarden van -L tot +L aannemen, inclusief 0. Dus, voor l =1 (p orbitalen), zijn er ml =-1, 0, +1, waardoor drie p -orbitalen langs de x-, y- en z -assen worden georiënteerd.
* Spin Quantum Number (MS): Beschrijft het intrinsieke hoekmomentum van een elektron, dat wordt gekwantiseerd en vaak wordt gevisualiseerd als het elektron "spinnen". Het kan +1/2 of -1/2 zijn.
2. AUFBAU -principe:
* Elektronen vullen orbitalen in volgorde van toenemende energie.
* De volgorde van vullen is gebaseerd op de diagonale regel (soms de Madelung -regel genoemd).
3. Pauli Exclusion Principle:
* Geen twee elektronen in een atoom kunnen dezelfde set van alle vier kwantumnummers hebben.
* Dit betekent dat elk orbitaal maximaal twee elektronen kan bevatten, met tegengestelde spins.
4. De regel van Hund:
* Binnen een subshell (bijv. De 2P -subshell) zullen elektronen elk orbitaal binnen die subshell afzonderlijk bezetten voordat ze worden gekoppeld.
* Dit maximaliseert het aantal ongepaarde elektronen en minimaliseert elektron-elektronenafstoting.
5. Elektronische configuratie:
De opstelling van elektronen in een atoom wordt de elektronische configuratie genoemd. Het is geschreven in de vorm:
(n) l^(aantal elektronen in die subshell)
De elektronische stikstofconfiguratie is bijvoorbeeld 1S² 2S² 2P³.
Voorbeeld:
Laten we eens kijken naar de elektronische configuratie van zuurstof (atoomnummer 8):
1. AUFBAU -principe: Volgens de diagonale regel vullen we de orbitalen in de volgorde 1, 2s, 2p.
2. Pauli Exclusion Principle: Elk orbitaal kan maximaal twee elektronen met tegengestelde spins bevatten.
3. De regel van Hund: Binnen de 2P -subshell plaatsen we één elektron in elk van de drie 2p -orbitalen voordat we elektronen koppelen.
Daarom is de elektronische configuratie van zuurstof:1S² 2S² 2P⁴
Opmerking: Deze regels bieden een raamwerk om te begrijpen hoe elektronen worden verdeeld over de kern. Het gedrag van elektronen is echter complex en de kwantummechanica speelt een belangrijke rol bij het verklaren van hun gedrag.
 De formule voor stikstofdioxide is NO2 Wat de molaire massa van het dichtstbijzijnde gram?
De formule voor stikstofdioxide is NO2 Wat de molaire massa van het dichtstbijzijnde gram?  Wat zijn de voedingsstoffen uit organische stoffen?
Wat zijn de voedingsstoffen uit organische stoffen?  Welke methode wordt gebruikt om erachter te komen of een middelenmetaal of niet-metaal?
Welke methode wordt gebruikt om erachter te komen of een middelenmetaal of niet-metaal?  Is Diamond samengesteld uit een enkel element?
Is Diamond samengesteld uit een enkel element?  Waarom verschillen de valance -elektronen van metaalbindingen van andere bindingen?
Waarom verschillen de valance -elektronen van metaalbindingen van andere bindingen?
 Spanningen nemen toe over kleine waterkrachtcentrales in Servië
Spanningen nemen toe over kleine waterkrachtcentrales in Servië Leg uit hoe dieren die in het bos wonen, het helpen groeien en regenereren?
Leg uit hoe dieren die in het bos wonen, het helpen groeien en regenereren?  Integratie van gezondheids- en klimaatagenda's
Integratie van gezondheids- en klimaatagenda's Sterke cycloon treft Oost-India, beïnvloedt Aziatisch subcontinent
Sterke cycloon treft Oost-India, beïnvloedt Aziatisch subcontinent Nieuw onderzoek suggereert minerale nanodeeltjes als alomtegenwoordige enzymnabootsers in aardse systemen
Nieuw onderzoek suggereert minerale nanodeeltjes als alomtegenwoordige enzymnabootsers in aardse systemen
Hoofdlijnen
- Waarom is de term immuunsysteem een verkeerde benaming?
- Wat is een andere naam voor een waarneembaar kenmerk of kenmerk van organisme?
- Hoe de snelste spier ter wereld vier unieke vogelsoorten creëerde
- Hoe natuurlijke kanaaleiwitten bewegen in kunstmatige membranen
- Onderzoekers ontdekken verschillende levenscyclusfasen van de ectosymbiotische DPANN-archaeon Nanobdella aerobiophila
- Hoe een klein deel van de oceanen in de wereld aan de mondiale vraag naar zeevruchten zou kunnen voldoen
- Wat is de structuur die eiwitten produceert?
- Hoe heten de cellen in neus en keel die stofdeeltjes opvangen?
- Wat zijn de negen menselijke systemen?
- Problemen met bellen vermijden:onderzoek naar de relatie tussen bellen en elektrochemie

- Drugsbibliothecaris ontdekt nieuwe stof die veelvoorkomende chirurgische complicaties kan dwarsbomen
- Eiwitporiën verpakt in polymeren maken superefficiënte filtratiemembranen

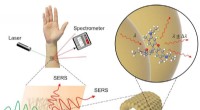
- Een nieuwe Raman chemische sensor gemaakt van noedelachtige draden van goud
- Flow chemie techniek biedt snellere, veiligere manier om te screenen, bestuderen en optimaliseren van industriële chemische reacties

 Drie manieren waarop bedrijven hun producten veranderen om inflatie te verbergen
Drie manieren waarop bedrijven hun producten veranderen om inflatie te verbergen  Waarom zou de rotslagen die vissen en andere zeeleven bevatten, op de top van de bergen worden gevonden?
Waarom zou de rotslagen die vissen en andere zeeleven bevatten, op de top van de bergen worden gevonden?  Stellaire slang gevonden in de kosmische buurt
Stellaire slang gevonden in de kosmische buurt Facebook-inkomsten dalen naarmate het gebruik tijdens pandemie stijgt
Facebook-inkomsten dalen naarmate het gebruik tijdens pandemie stijgt Het conventionele begrip van antivries-eiwitten in twijfel trekken
Het conventionele begrip van antivries-eiwitten in twijfel trekken Hoe de uitstoot van voedselproductie de gezondheid schaadt
Hoe de uitstoot van voedselproductie de gezondheid schaadt  Die uitstekende T Rex-tanden? Ze waren bedekt met lippen:studie
Die uitstekende T Rex-tanden? Ze waren bedekt met lippen:studie  Bio vliegtuigbrandstoffen goed voor het klimaat, maar technologieën moeten worden aangepast
Bio vliegtuigbrandstoffen goed voor het klimaat, maar technologieën moeten worden aangepast
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

