
Wetenschap
Drugsbibliothecaris ontdekt nieuwe stof die veelvoorkomende chirurgische complicaties kan dwarsbomen
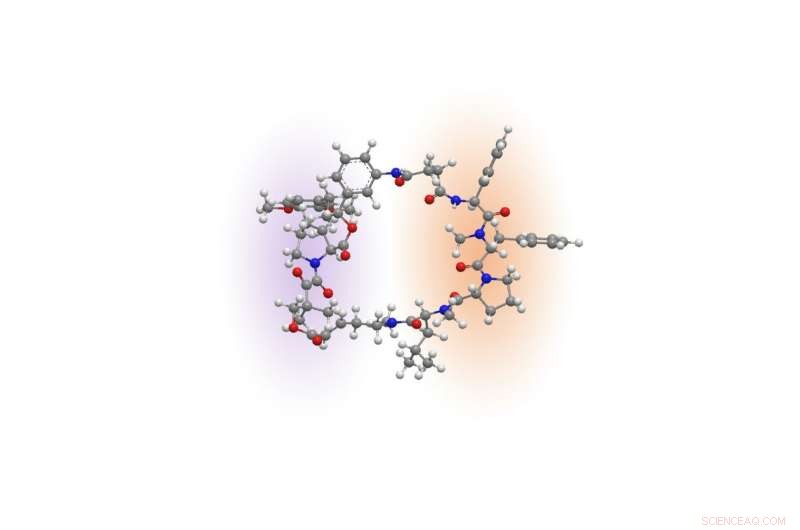
Rapadocine molecuul. Krediet:Liu-laboratorium
Bij een strategische zoektocht Johns Hopkins-wetenschappers creëerden en screenden een bibliotheek van 45, 000 nieuwe verbindingen die chemische elementen bevatten van veelgebruikte onderdrukkers van het immuunsysteem, en zeggen dat ze er een hebben gevonden die reperfusieschade kan voorkomen, een weefselbeschadigende en veel voorkomende complicatie van chirurgie, hartaanval en beroerte.
Het Johns Hopkins-team noemde zijn nieuw ontdekte verbinding rapadocine en heeft er patenten op ingediend en zijn familie van 45, 000 chemische neven. Het heeft het medicijn ook in licentie gegeven aan het in Baltimore gevestigde biotechnologiebedrijf Rapafusyn Pharmaceuticals, die mede werd opgericht door de leider van de studie, juni O. Liu, doctoraat, een professor in farmacologie en oncologie aan de Johns Hopkins University School of Medicine. De onderzoekers waarschuwen dat elke commercialisering of klinisch gebruik van het medicijn moet wachten op substantiële verdere veiligheids- en voordelenstudies bij mensen.
Een rapport over de methode die wordt gebruikt om rapadocine te maken en te identificeren, evenals laboratoriumtests ervan bij muizen met reperfusieletsels in hun nieren verschenen op 10 december Natuurchemie .
"Reperfusieletsels zijn een veel voorkomende complicatie na een operatie, vooral bij ouderen, ", zegt Liu, die toezicht houdt op een bibliotheek van duizenden van 's werelds ooit gebruikte medicijnen in de Johns Hopkins Drug Library.
Het letsel treedt op wanneer, na de operatie, artsen maken klemmen op bloedvaten los en een golf van zuurstofrijk bloed stroomt terug naar weefsels die er tijdelijk van uitgehongerd waren. De golf van bloed kan de weefsels schokken en ontstekingen en orgaanschade veroorzaken. De aandoening kan ook optreden wanneer verstopte slagaders worden geopend na hartaanvallen en beroertes. Momenteel, er wordt een aantal medicijnen bestudeerd om reperfusieletsels te behandelen, en sommige behandelingen, zoals bloedverdunners en ontstekingsremmende medicijnen, kan licht effectief zijn voor bepaalde soorten van de aandoening.
Om het nieuwe medicijn te vinden, Liu, die co-directeur is van het Cancer Chemical and Structural Biology Program in het Johns Hopkins Kimmel Cancer Center, herinnerde zich zijn postdoctorale opleidingsjaren waarin hij bestudeerde hoe een medicijn genaamd rapamycine werkt. Eigenlijk, het onderdrukt het immuunsysteem en wordt vaak voorgeschreven aan niertransplantatiepatiënten om afstoting van hun nieuwe organen te voorkomen.
"Ik heb altijd gedacht dat rapamycine interessante eigenschappen had, " zegt Liu. "Het is erg stabiel en cellen kunnen er grote hoeveelheden van opnemen, vooral vanwege de chemische structuur."
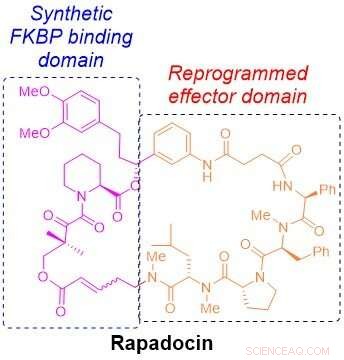
De moleculaire structuur van rapadocine. Krediet:Liu-laboratorium
chemisch, rapamycine en een ander immunosuppressivum, genaamd FK506, bevatten een unieke steiger die bijna de helft van een ring vormt. Die helft van de ring, het FKBP-bindende domein genoemd, is bijna identiek tussen de twee geneesmiddelen, en de andere helft het zogenaamde effectordomein, is voor elk van hen uniek. Het FKBP-bindende domein van de geneesmiddelen biedt een aantal voordelen, inclusief stabiliteit en grotere verdeling door het lichaam. Het effectordomein zorgt ervoor dat elk medicijn zich op een ander eiwit richt om het immuunsysteem te onderdrukken of de groei van kankercellen te remmen.
Geïnspireerd door de unieke chemische architecturen van rapamycine en FK506, Liu vroeg zich af of het mogelijk was om soortgelijke ringvormige moleculen te bouwen door het effectordomein van rapamycine uit te wisselen en te vervangen door nieuwe bouwstenen om andere eiwitten aan te pakken die betrokken zijn bij menselijke ziekten.
Om dit te doen, Liu en zijn team maakten 45, 000 combinaties van verbindingen met een FKBP-bindend domein en verschillende effectordomeinen. "We hadden veel meer combinaties kunnen maken, maar had slechts een bepaalde hoeveelheid middelen om mee te werken, " herinnert Liu zich.
Liu en zijn team verdeelden de enorme pool van 45, 000 verbindingen in 3, 000 kleinere groepen en testten elke groep op degenen die een chemische route blokkeerden die verband hield met reperfusieschade.
Dat pad is een pompsysteem genaamd equilibrative nucleoside transporter, of KNO, die een molecuul transporteert dat adenosine wordt genoemd, een belangrijke biologische boodschapper, de cel in. Weefsels die uitgehongerd zijn voor zuurstof produceren grote hoeveelheden adenosine. Adenosine beschermt cellen tegen schade door verbinding te maken met receptoren op het oppervlak van cellen. Om te bepalen hoeveel en hoe lang adenosine verbinding maakt met zijn receptor, cellen kunnen de activiteit van adenosine dempen door het via de KNO-transporter in de cel te slikken. "Dus het doel is om adenosine langer buiten de cel te houden om reperfusieletsels te behandelen, " zegt Liu.
Om adenosine buiten de cel te houden, de wetenschappers zochten naar de verbindingen die de KNO-activiteit blokkeerden en hielden de meeste adenosine buiten de cellen om het weefselbeschermende effect zo lang mogelijk te behouden. Eén verbinding bereikte de top van hun experimenten, en ze noemden het rapadocin.
In laboratoriumstudies van 25 muizen, de wetenschappers injecteerden hen met rapadocine, verwijderden een van hun nieren en klemden de andere gedurende 45 minuten vast; 24 uur later, ze bemonsterden hun bloed voor niveaus van creatinine en stikstof, die markers zijn van reperfusieschade.
De dieren die rapadocine kregen, hadden een derde minder creatinine (0,4 milligram per deciliter vergeleken met 0,6 milligram per deciliter gemiddeld) en minder dan de helft van het stikstofgehalte (40 milligram per deciliter vergeleken met 90 milligram per deciliter gemiddeld) dan controlemuizen die een medicijn gegeven om de effecten van rapadocine teniet te doen.
 Kritieke grondwatervoorraden herstellen mogelijk nooit van droogte
Kritieke grondwatervoorraden herstellen mogelijk nooit van droogte Luchtvervuiling scheert jaren uit het leven van mensen, studie vondsten
Luchtvervuiling scheert jaren uit het leven van mensen, studie vondsten Schotse rivieren kunnen drie keer zoveel droogtes krijgen
Schotse rivieren kunnen drie keer zoveel droogtes krijgen Dodental orkanen in Puerto Rico op bijna 3 000
Dodental orkanen in Puerto Rico op bijna 3 000 Klimaatexperts zeggen dat ze praten bij de VN, maar niet veel actie
Klimaatexperts zeggen dat ze praten bij de VN, maar niet veel actie
Hoofdlijnen
- Laat je huisdier niet per ongeluk dronken worden dit gekke seizoen (sorry Tiddles)
- Wat moet er gebeuren met de DNA-strengen in de kern voordat de cel kan delen?
- Kikker en menselijke bloedcellen vergelijken en identificeren
- Cilia: definitie, types en functie
- Pittige Tomaten,
- Wat hebben piranha's en goudvissen gemeen?
- Een enzym dat de vorming van het DNA katalyseert Molecuul
- Heeft Kelp veel verschillende cellen?
- Welke bijdrage heeft Avery geleverd aan de ontdekking van DNA?
- Detectie van antilichamen met gloeiende eiwitten, draad en een smartphone

- Wetenschappers ontwerpen materiaal dat energie kan opslaan als een adelaarsgreep
- Annotatietool biedt een stap in de richting van het begrijpen van verbanden tussen ziekte, gemuteerd RNA
- Veilig printen met onzichtbare inkt op waterbasis

- Ionische verbindingen noemen

 Gedaan met vissen:onderzoekers beeldvormende techniek trollen in stille cellulaire zeeën
Gedaan met vissen:onderzoekers beeldvormende techniek trollen in stille cellulaire zeeën Chemici bereiken doorbraak in de synthese van grafeen nanoribbons
Chemici bereiken doorbraak in de synthese van grafeen nanoribbons Nanomagneten bieden stof tot nadenken over computergeheugens
Nanomagneten bieden stof tot nadenken over computergeheugens Kostbare vorst in Frankrijk toegeschreven aan klimaatverandering
Kostbare vorst in Frankrijk toegeschreven aan klimaatverandering Koeltechnologie om de levensvatbaarheid van het gekoelde muizensperma gedurende 10 dagen te behouden
Koeltechnologie om de levensvatbaarheid van het gekoelde muizensperma gedurende 10 dagen te behouden Europese luchtvaartmaatschappijen zoeken groter stuk Latijns-Amerikaanse taart
Europese luchtvaartmaatschappijen zoeken groter stuk Latijns-Amerikaanse taart Studie onderzoekt wanneer en waarom steekpenningen invloed kopen, en wat hun effectiviteit vermindert?
Studie onderzoekt wanneer en waarom steekpenningen invloed kopen, en wat hun effectiviteit vermindert? Worden je hersenen moe zoals de rest van je lichaam?
Worden je hersenen moe zoals de rest van je lichaam?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | German | Dutch | Danish | Norway | Swedish |

-
Wetenschap © https://nl.scienceaq.com

