
Wetenschap
Welke vaste stoffen hebben een willekeurige opstelling van deeltjes?
Dit is waarom:
* kristallijne vaste stoffen Heb een sterk geordend, herhaaldelijk patroon van deeltjes (denk aan een perfecte, symmetrische kristalstructuur). Deze volgorde strekt zich uit over de hele vaste stof.
* Amorfe vaste stoffen , aan de andere kant, ontbreekt deze langeafstandsvolgorde. Hun deeltjes zijn op een meer willekeurige, ongeorganiseerde manier gerangschikt.
Voorbeelden van amorfe vaste stoffen:
* glas: Hoewel het vast aanvoelt, is glas eigenlijk een zeer viskeuze vloeistof. De moleculen zijn op een ongeordende manier gerangschikt, waardoor het zijn karakteristieke brosheid en gebrek aan een gedefinieerd smeltpunt heeft.
* rubber: Rubber is flexibel en kan strekken omdat de moleculen willekeurig met elkaar verweven zijn.
* Plastic: Veel kunststoffen zijn amorf, met moleculen gerangschikt in een niet-herhalend patroon.
* gelatine: Deze eiwitgebaseerde stof vormt een ongeordende vaste structuur.
Het is belangrijk op te merken dat zelfs binnen amorfe vaste stoffen er misschien een lokale volgorde is, maar deze volgorde strekt zich niet uit in het hele materiaal zoals in kristallijne vaste stoffen.
 Is koperacetaat een zwakke base?
Is koperacetaat een zwakke base?  Op afstand bestuurde medicijnafgifte implantaatgrootte van druif kan helpen bij het beheer van chronische ziekten
Op afstand bestuurde medicijnafgifte implantaatgrootte van druif kan helpen bij het beheer van chronische ziekten Insectenantibioticum biedt nieuwe manier om bacteriën te elimineren
Insectenantibioticum biedt nieuwe manier om bacteriën te elimineren Hoeveel mol zijn er in 125,00 gram natriumsulfide?
Hoeveel mol zijn er in 125,00 gram natriumsulfide?  Wat zijn alle koolwaterstoffen en hun derivaten?
Wat zijn alle koolwaterstoffen en hun derivaten?
Hoofdlijnen
- Hoe definieer je haat?
- Waar komt ons hoofd vandaan?
- Wat is het proces van het behoud van dode dieren voor dissectie?
- Cellen in de speekselklieren en alvleesklier die grote hoeveelheden eiwitten scheiden, hebben een sterk ontwikkelde wat?
- Wat is het eindproduct van fotosynthese?
- Etiketten op verpakt vlees die de versheid weergeven, kunnen de houdbaarheidsdata vervangen, waardoor voedselverspilling wordt verminderd
- Differentiële effecten van volwassen bomen op nakomelingen en niet-nakomelingen in een subtropisch bos
- Kunnen condors terugkeren naar Noord-Californië?
- Wat heeft meer organismen een meer of vijver?
- Onderzoekers krijgen nieuwe inzichten in een dynamisch eiwit gericht op kankertherapie
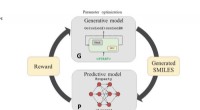
- Kunstmatig-intelligentiesysteem ontwerpt medicijnen helemaal opnieuw
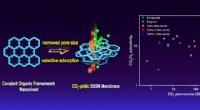
- Eenfasige covalente organische raamwerkmembranen maken CO2-selectieve scheiding mogelijk
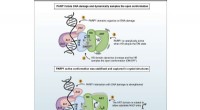
- Onderzoek zoomt in op enzym dat DNA-schade door UV-stralen herstelt

- Onderzoekers ontwikkelen semi-vloeibare metaalanode voor batterijen van de volgende generatie

 Hoe werken de hersenen samen met andere organen in je lichaam?
Hoe werken de hersenen samen met andere organen in je lichaam?  Brengt een vulkaan rustig uit als zijn magma dik en plakkerig is?
Brengt een vulkaan rustig uit als zijn magma dik en plakkerig is?  Onderzoeken hoe antibioticaresistente bacteriën agressief worden
Onderzoeken hoe antibioticaresistente bacteriën agressief worden  Atomair nauwkeurige nanocluster kan nieuwe richting geven aan nanokatalysatoren
Atomair nauwkeurige nanocluster kan nieuwe richting geven aan nanokatalysatoren Waarom tapdansen vervende gifkikkers?
Waarom tapdansen vervende gifkikkers?  Hoe het domein van een vierkantswortelfunctie te vinden
Hoe het domein van een vierkantswortelfunctie te vinden Waarom was orkaan Lane zo onvoorspelbaar?
Waarom was orkaan Lane zo onvoorspelbaar?  Kleine motoren zetten een grote stap voorwaarts
Kleine motoren zetten een grote stap voorwaarts
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

