
Wetenschap
Hoe wordt de oplosbaarheid van gassen in vloeistoffen beïnvloed door temperatuurveranderingen?
1. Kinetische energie en ontsnapping:
* Verhoogde temperatuur Middelen moleculen in zowel de vloeistof- als gasfasen hebben hogere kinetische energie.
* Deze verhoogde energie maakt het gemakkelijker voor de gasmoleculen die in de vloeistof werden opgelost om de aantrekkelijke krachten te overwinnen die ze in oplossing houden en terug in de gasfase ontsnappen.
2. Verminderde intermoleculaire krachten:
* Bij hogere temperaturen bewegen de vloeibare moleculen sneller en verzwakken de intermoleculaire krachten tussen hen.
* Dit maakt het moeilijker voor de gasmoleculen om te interageren met de vloeibare moleculen en opgelost te blijven.
3. Drukeffecten:
* Temperatuur beïnvloedt indirect gasoplosbaarheid door druk. Naarmate de temperatuur toeneemt, neemt de dampdruk van het gas boven de vloeistof ook toe.
* Deze hogere dampdruk duwt meer van het opgeloste gas uit de oplossing.
Voorbeelden:
* Een fles frisdrank openen: Je zult merken dat een warme frisdrank snel plat gaat. Dit komt omdat de verhoogde temperatuur ervoor zorgt dat het opgeloste kooldioxidegas ontsnapt.
* kokend water: Wanneer u water kookt, worden de opgeloste gassen (zoals zuurstof en stikstof) in de lucht uitgezet.
Praktische implicaties:
* Vis en waterleven: Warmer water bevat minder opgeloste zuurstof, waardoor het moeilijk is voor vissen en andere waterorganismen om te overleven.
* Klimaatverandering: Ocean Warming zorgt ervoor dat de oplosbaarheid van CO2 afneemt, wat bijdraagt aan een positieve feedbacklus die de klimaatverandering versnelt.
* Chemische reacties: Temperatuur kan worden gebruikt om de oplosbaarheid van gassen in industriële processen te regelen, wat de reactiesnelheden en opbrengsten beïnvloedt.
Key Takeaway: Zie het zo:warmte maakt de gasmoleculen "willen" uit de vloeistof ontsnappen, zoals proberen uit een drukke, warme kamer te komen.
 Houding heeft invloed op hoe u uw eten waarneemt
Houding heeft invloed op hoe u uw eten waarneemt  Aanpassen aan klimaatverandering:deden het verkeerd
Aanpassen aan klimaatverandering:deden het verkeerd Massale evacuaties als grote cycloon op weg naar Zuid-Azië
Massale evacuaties als grote cycloon op weg naar Zuid-Azië Wereldmeren verliezen snel zuurstof naarmate de planeet opwarmt
Wereldmeren verliezen snel zuurstof naarmate de planeet opwarmt Klokken raken op door klimaatverandering. Californië zegt dat het tijd is voor gigantische koolstofstofzuigers
Klokken raken op door klimaatverandering. Californië zegt dat het tijd is voor gigantische koolstofstofzuigers
Hoofdlijnen
- Wat draagt het meest bij aan de vervuiling?
- Zelfvernietiging van muggen
- Welk systeem voert de organische functies uit van inname -digestie en uitscheiding?
- Welke systemen maken het voor een mens mogelijk om te schrijven en hoe?
- Wat maakt de dodelijke kogelvis zo verrukkelijk?
- Wat zijn de twee factoren die de efficiëntie van een enzym beïnvloeden?
- Nieuw onderzoek heeft uitgewezen dat virussen ogen en oren op ons kunnen richten
- Functies van het bloedsomloopstelsel
- Wat is zoetwaterbiota?
- Deconstructie van het superfood dat de honingbijhiërarchie bepaalt

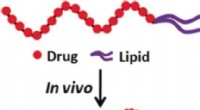
- Transport van lipide-geconjugeerd floxuridine door natuurlijk serumalbumine voor levering aan kankercellen
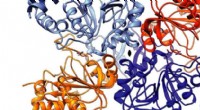
- Wetenschappers breken de structuur van tuberculose af
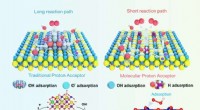
- Ontwerpstrategie op moleculair niveau kan de sleutel zijn tot het stimuleren van commerciële waterstofproductie
- Het terugwinnen van fosfor uit de productie van maïs-ethanol kan de grondwatervervuiling helpen verminderen

 Zijn opgenomen observaties en wetenschappelijke resultaten hetzelfde?
Zijn opgenomen observaties en wetenschappelijke resultaten hetzelfde?  Onderzoek maakt fysica van glasvorming duidelijker
Onderzoek maakt fysica van glasvorming duidelijker Hoe is de technologie verbeterd?
Hoe is de technologie verbeterd?  Te moeilijk om aan het werk te gaan:klimaatverandering maakt het leven van werknemers moeilijker
Te moeilijk om aan het werk te gaan:klimaatverandering maakt het leven van werknemers moeilijker  Wat is een voorbeeld van een synthetisch polymeer?
Wat is een voorbeeld van een synthetisch polymeer?  Zijn er uitgestorven vulkanen in Cuba?
Zijn er uitgestorven vulkanen in Cuba?  Verontreinigende stoffen uit water verwijderen met stuifmeel en sporen - zonder de achoo!
Verontreinigende stoffen uit water verwijderen met stuifmeel en sporen - zonder de achoo! Van chemische grafieken tot structuren
Van chemische grafieken tot structuren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

