
Wetenschap
Wat is het smeltpunt van de zoutoplossing?
* Het specifieke zout: Verschillende zouten hebben verschillende smeltpunten. Natriumchloride (tafelzout) heeft bijvoorbeeld een smeltpunt van 801 ° C, terwijl kaliumchloride een smeltpunt van 770 ° C heeft.
* De concentratie van het zout: Naarmate de zoutconcentratie in de oplossing toeneemt, neemt het smeltpunt af. Dit komt omdat de zoutionen interfereren met de vorming van het ijskristalrooster.
* De aanwezigheid van andere opgeloste stoffen: De aanwezigheid van andere opgeloste stoffen in de oplossing kan ook het smeltpunt beïnvloeden.
Daarom is het onmogelijk om een enkel smeltpunt te geven voor een zoutoplossing.
We kunnen echter het volgende zeggen:
* Zoutoplossingen hebben over het algemeen een lager smeltpunt dan zuiver water (0 ° C).
* Hoe lager de zoutconcentratie, hoe dichter het smeltpunt tot 0 ° C zal zijn
Voorbeeld:
Een zoutoplossing van 10% heeft een smeltpunt rond -6 ° C. Een zoutoplossing van 20% heeft een smeltpunt rond -12 ° C.
Opmerking:
Het smeltpunt van een zoutoplossing wordt ook beïnvloed door de druk. Dit effect is echter meestal te verwaarlozen bij atmosferische druk.
 Hoe chemische aanwijzingen van prehistorische microben het verhaal herschreven van een van de grootste massa-extincties op aarde
Hoe chemische aanwijzingen van prehistorische microben het verhaal herschreven van een van de grootste massa-extincties op aarde Hoe het verschil te zien tussen mannelijke en vrouwelijke bloemen
Hoe het verschil te zien tussen mannelijke en vrouwelijke bloemen Wetenschappers verzamelen de poep van aardvarkens om te begrijpen hoe de soort wordt beïnvloed door het klimaat in Afrika
Wetenschappers verzamelen de poep van aardvarkens om te begrijpen hoe de soort wordt beïnvloed door het klimaat in Afrika  Satellietweergave van post-tropische cycloon Jose die aan het vervagen is
Satellietweergave van post-tropische cycloon Jose die aan het vervagen is NASA ziet tropische cycloon 02S zich ontwikkelen in de Zuidelijke Indische Oceaan
NASA ziet tropische cycloon 02S zich ontwikkelen in de Zuidelijke Indische Oceaan
Hoofdlijnen
- Wat is het organisme dat dood en levend is?
- Hoe menselijke migratie werkt
- Wat maakt een verhaal succesvol? Onderzoekers hebben een manier gevonden om dit te voorspellen
- Dominant Allele: wat is het? & Waarom gebeurt het? "(with Traits Chart)
- Ondergaat elk levend ding aseksuele reproductie?
- Beschrijf de ontdekkingen die hebben geleid tot het modelleren van DNA?
- Houdt mijn hond echt van mij?
- Wat zijn de negen menselijke systemen?
- Zegt de wet van segregatie en recombinatie dat?
- Een sleutel tot goedkopere hernieuwbare brandstoffen:voorkomen dat ijzer gaat roesten

- UNT's moderne alchemist zet eerste stappen om methaan om te zetten in methanol
- Lichtgevoelige toplaag van plastic folie zorgt voor beweging

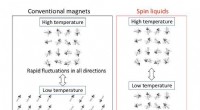
- Van overvloedige koolwaterstoffen tot zeldzame spinvloeistoffen
- Freeze frame:onderzoekers lossen op hoe cellen eiwitten ontvouwen
 Bij constante druk neemt een vaste gasmassa een volume in van 20 m3 bij 27 ° C. Het temperatuursysteem werd verhoogd naar 177. Bereken is er nieuw gas ingenomen?
Bij constante druk neemt een vaste gasmassa een volume in van 20 m3 bij 27 ° C. Het temperatuursysteem werd verhoogd naar 177. Bereken is er nieuw gas ingenomen?  Het opzetten van een buiten-tv of -projector is eenvoudiger geworden
Het opzetten van een buiten-tv of -projector is eenvoudiger geworden Is Newton of Kelvin de SI -eenheid voor temperatuur?
Is Newton of Kelvin de SI -eenheid voor temperatuur?  Zou het binnenkort game-over kunnen zijn voor de Fortnite-rage?
Zou het binnenkort game-over kunnen zijn voor de Fortnite-rage?  Als je een metaal en vloeistof bent, wat ben je dan?
Als je een metaal en vloeistof bent, wat ben je dan?  Digitale fotografie:de toekomst van kleinschalige productie?
Digitale fotografie:de toekomst van kleinschalige productie?  Klimaattechniek, eens begonnen, zou ernstige gevolgen hebben als gestopt
Klimaattechniek, eens begonnen, zou ernstige gevolgen hebben als gestopt NASA-satelliet geeft zicht op grote orkaan Humberto
NASA-satelliet geeft zicht op grote orkaan Humberto
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

