
Wetenschap
Hoe brengt u S HNO3 in evenwicht H2SO4 NO2 H2O?
Dit is waarom en hoe de juiste reactie te vertegenwoordigen:
De daadwerkelijke reactie:
Zwavel (S) reageert met geconcentreerd salpeterzuur (HNO₃) om zwavelzuur (H₂SO₄) en stikstofdioxide (NO₂) te vormen. Dit is een oxidatie-reductiereactie waarbij zwavel wordt geoxideerd tot sulfaat en salpeterzuur wordt gereduceerd tot stikstofdioxide.
De evenwichtige vergelijking:
De juiste evenwichtige chemische vergelijking voor deze reactie is:
s + 6 hno₃ → h₂so₄ + 6 no₂ + 2 h₂o
Verklaring van evenwicht:
1. zwavel (s): Er is één zwavelatoom aan elke kant.
2. waterstof (H): Er zijn zes waterstofatomen aan de linkerkant (van HNO₃) en twee rechts (van H₂so₄ en H₂o).
3. stikstof (n): Er zijn zes stikstofatomen aan de linkerkant (van HNO₃) en zes rechts (van NO₂).
4. zuurstof (O): Er zijn 18 zuurstofatomen aan de linkerkant (van Hno₃) en 18 rechts (van H₂so₄, No₂ en H₂o).
Sleutelpunten:
* Deze reactie vereist geconcentreerd salpeterzuur als het oxidatiemiddel.
* De reactie is zeer exotherme en produceert een aanzienlijke hoeveelheid warmte.
* De producten, zwavelzuur en stikstofdioxide, zijn zeer corrosief en giftig.
Laat het me weten als je andere chemische reacties hebt die je zou willen in evenwicht brengen!
 Gelijktijdig optredende verontreinigingen kunnen NC-grondwaterrisico's vergroten
Gelijktijdig optredende verontreinigingen kunnen NC-grondwaterrisico's vergroten Verandert de klimaatverandering de vakantieplannen van mensen?
Verandert de klimaatverandering de vakantieplannen van mensen?  Nieuw wasmachinefilter breekt plastic microvezels af
Nieuw wasmachinefilter breekt plastic microvezels af Met stormen in mei, wetgever wil een langer orkaanseizoen
Met stormen in mei, wetgever wil een langer orkaanseizoen Aardbevingsfouten hebben mogelijk een sleutelrol gespeeld bij het vormgeven van de cultuur van het oude Griekenland
Aardbevingsfouten hebben mogelijk een sleutelrol gespeeld bij het vormgeven van de cultuur van het oude Griekenland
Hoofdlijnen
- Hoe ziet de binnenkant van een stamcel eruit?
- Wat is de plantenvoedsel dat een soort suiker wordt genoemd?
- Wat zijn indicatoren voor cultuur?
- Hoe snelheid de evolutionaire verandering van de wervelkolom bij zoogdieren beperkt
- De wetenschappelijke studie van het menselijke skelet?
- Waarom is het belangrijk om een bacteriecultuur te starten met een enkele geïsoleerde kolonie?
- Waarom falen de besturen van sommige organisaties? Het kan zijn hoe bestuurders hun expertise en verantwoordelijkheden waarnemen
- Hebben eiercellen chemicaliën op het puntje van het hoofd?
- Dode bomen leven met schimmels
- Hoe oude banden te mixen en puin aan te leggen om duurzame wegen te maken

- AI versterkt vegetarische hamburgers terwijl de markt groeit

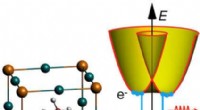
- Licht schijnend op recombinatiemechanismen in zonnecelmaterialen
- Nieuw membraanwaterbehandelingssysteem om giftig afval en afvalverwerkingskosten met meer dan 90 procent te verminderen

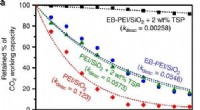
- Onderzoekers produceren 50x stabieler adsorbens
 Welke term beschrijft opgeslagen energie?
Welke term beschrijft opgeslagen energie?  Canada kan zich beter voorbereiden op het omscholen van werknemers die ontheemd zijn door disruptieve technologieën
Canada kan zich beter voorbereiden op het omscholen van werknemers die ontheemd zijn door disruptieve technologieën Welke drie dingen stelt de oorspronkelijke celtheorie voor?
Welke drie dingen stelt de oorspronkelijke celtheorie voor?  Draagkracht in een ecosysteem
Draagkracht in een ecosysteem Onderzoekers creëren transparante, rekbare geleiders met nano-accordeonstructuur
Onderzoekers creëren transparante, rekbare geleiders met nano-accordeonstructuur In welk sterrenbeeld heeft Big Dipper gevonden?
In welk sterrenbeeld heeft Big Dipper gevonden?  Nieuw werk breidt de thermodynamische rekentheorie uit
Nieuw werk breidt de thermodynamische rekentheorie uit  Welke maan zou er de helderste uit het oppervlak van Jupiter uit Lo Europa Ganymede en Callisto uitzien waarom?
Welke maan zou er de helderste uit het oppervlak van Jupiter uit Lo Europa Ganymede en Callisto uitzien waarom?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

