
Wetenschap
Wanneer een metaal reageert met niet -metaal, zijn de stoffen goede geleiders van elektrische stroom?
* metalen zijn uitstekende elektriciteitsgeleiders. Dit komt door hun vrij bewegende elektronen.
* Niet -metalen zijn over het algemeen slechte elektriciteitsgeleiders. Ze hebben de neiging om hun elektronen stevig vast te houden, waardoor het voor elektronen moeilijk is om vrij te stromen.
Wanneer een metaal reageert met een niet -metaal, vormen ze een ionische verbinding. Ionische verbindingen worden gevormd door de overdracht van elektronen van het metaal naar het niet -metaal.
* ionische verbindingen, in hun vaste toestand, zijn meestal slechte elektriciteitsgeleiders. De ionen worden gehouden in een rigide roosterstructuur en hebben niet de vrijheid om te bewegen en een elektrische stroom te dragen.
* Ionische verbindingen opgelost echter opgelost in water (vormen een elektrolytoplossing) worden goede geleiders. De ionen worden vrij om in de oplossing te bewegen, waardoor de stroom van elektrische stroom mogelijk is.
Samenvattend:
* Het metaal zelf blijft een goede geleider.
* Het niet -metaal zelf blijft een slechte geleider.
* De gevormde ionische verbinding is over het algemeen een slechte geleider in zijn vaste toestand, maar kan een goede geleider zijn wanneer het in water is opgelost.
Voorbeeld:
* natrium (metaal) + chloor (niet -metaal) -> natriumchloride (NaCl) (ionische verbinding)
* Solide NaCl is een slechte geleider.
* NaCl opgelost in water is een goede geleider.
 Welke producten zijn gemaakt van zuur?
Welke producten zijn gemaakt van zuur?  Wat is de vergelijking van zilversulfidevormen wanneer en zwavel reageren?
Wat is de vergelijking van zilversulfidevormen wanneer en zwavel reageren?  Test op levensbedreigend voedingstekort wordt gemaakt van ingewanden van bacteriën
Test op levensbedreigend voedingstekort wordt gemaakt van ingewanden van bacteriën Welke elektronenconfiguratie is correct voor een natriumion?
Welke elektronenconfiguratie is correct voor een natriumion?  Is het bevriezen van koolstofdioxide een chemische verandering of een fysieke verandering?
Is het bevriezen van koolstofdioxide een chemische verandering of een fysieke verandering?
 Duitsland geeft toe dat het de klimaatdoelstelling voor 2020 ver achterblijft
Duitsland geeft toe dat het de klimaatdoelstelling voor 2020 ver achterblijft Nieuwe studie:hoeveel invloed hebben klimaatschommelingen op de mondiale gewasopbrengsten?
Nieuwe studie:hoeveel invloed hebben klimaatschommelingen op de mondiale gewasopbrengsten?  Hoes, krimpen, verbouwen? Methoden voor biologische bodembedekkers onderzocht voor onkruidbestrijding
Hoes, krimpen, verbouwen? Methoden voor biologische bodembedekkers onderzocht voor onkruidbestrijding Branden in Athene behoren tot de dodelijkste in Europa deze eeuw
Branden in Athene behoren tot de dodelijkste in Europa deze eeuw Greening the greyfields:hoe onze buitenwijken te vernieuwen voor meer leefbare, net-zero steden
Greening the greyfields:hoe onze buitenwijken te vernieuwen voor meer leefbare, net-zero steden
Hoofdlijnen
- Wat hebben piranha's en goudvissen gemeen?
- Remming van het belangrijkste metabolische enzym toont belofte tegen melanoom
- Eens in de eeuw bloeien en zaaien van dwergbamboe verhoogt de muizenpopulaties
- Binaire splijting: definitie & proces
- Wat is het primaire niveau van een eiwitstructuur?
- Waarom zijn strikte aërobe oxidase positief?
- Zijn er mitochondriën in een dierlijke cel?
- Hoe worden binnendringende bacteriën vernietigd?
- Was deze hyena een verre voorouder van de hedendaagse termietenetende aardwolf?
- Werken om nieuwe behandelingen voor tuberculose te ontdekken
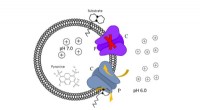
- Oppervlaktechemie onthult bijtende geheimen

- Onderzoekers ontdekken proces om psilocybine duurzaam te produceren een kandidaat-geneesmiddel dat kan helpen bij de behandeling van depressie

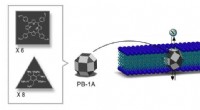
- Synthetische nanokanalen voor jodidetransport
- Op mosselen geïnspireerde lijm kan op een dag foetale chirurgie veiliger maken

 Is verdamping van geest op de huid een fysieke verandering?
Is verdamping van geest op de huid een fysieke verandering?  Hoe chaostheorie werkt
Hoe chaostheorie werkt  Hoe groot zijn Mars en Jupiter Saturnus Uranus Neptunus Pluto?
Hoe groot zijn Mars en Jupiter Saturnus Uranus Neptunus Pluto?  Het evolutionaire voordeel van wenkbrauwen
Het evolutionaire voordeel van wenkbrauwen Genen en omgeving hebben een gelijke invloed bij het leren van rijke en arme kinderen, studie vondsten
Genen en omgeving hebben een gelijke invloed bij het leren van rijke en arme kinderen, studie vondsten Wat is de kleur van de maan een ster?
Wat is de kleur van de maan een ster?  Hoe de verwijdering van de Elwha-dam de riviermonding veranderde?
Hoe de verwijdering van de Elwha-dam de riviermonding veranderde? Hoe de lineaire beelden van een cirkel te berekenen
Hoe de lineaire beelden van een cirkel te berekenen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

