
Wetenschap
Synthetische nanokanalen voor jodidetransport
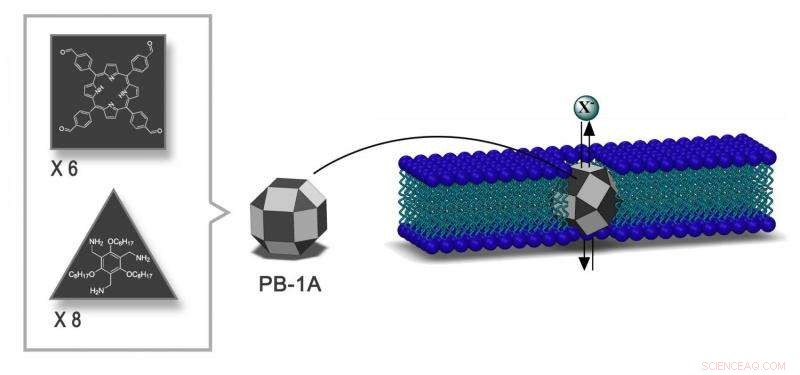
3D-structuur van de synthetische jodide-transporter PB-1A ontwikkeld door IBS-onderzoekers. Het PB-1A-ontwerp volgt de vorm van een veelvlak met 26 gezichten, gemaakt van driehoeken en vierkanten (donkergrijs) met 12 vlakken die leeg zijn gelaten als vensters (lichtgrijs) waar ionen doorheen kunnen. Het heeft een diameter van 3,64 nm en de juiste chemische eigenschappen om op het celmembraan te passen. Krediet:Instituut voor Basiswetenschappen
Uitwisseling van jodide (jodium-ionen) tussen bloedbaan en cellen is cruciaal voor de gezondheid van verschillende organen en het slecht functioneren ervan is gekoppeld aan struma, hypo- en hyperthyreoïdie, borstkanker, en maagkanker. Onderzoekers van het Centrum voor Zelfassemblage en Complexiteit, hebben binnen het Institute for Basic Science (IBS) nanostructuren bedacht die fungeren als kanalen voor jodidetransport in celmembranen. Deze studie, gepubliceerd in de Tijdschrift van de American Chemical Society ( JACS ), kan leiden tot diagnose en behandeling van jodidetransportstoornissen.
Een eiwit dat bekend staat als een natrium/jodide symporter (NIS) medieert het transport van jodide uit de bloedbaan naar schildkliercellen en andere weefsels, inclusief borstklieren tijdens borstvoeding, kankerachtige borstweefsels, en traanklieren. NIS is een holle structuur die de hoogte van het celmembraan overspant waardoor jodide in de cellen kan komen.
IBS-wetenschappers ontwikkelden synthetische ionenkanalen die selectief de doorgang van negatief geladen ionen mogelijk maken, vooral jodiden. Met een diameter van 3,64 nm en de juiste chemische eigenschappen, deze kanalen worden porfyrineboxen 1A (PB-1A) genoemd, passen in het celmembraan.
PB-1A heeft de vorm van een 26-vlaks veelvlak gemaakt van driehoeken en vierkanten, rhombicuboctaëder genoemd door Archimedes. Twee soorten moleculen vormen 14 vlakken van de vaste stof, terwijl de andere vlakken leeg worden gelaten zodat de ionen er doorheen kunnen.
PB-1A heeft het voordeel dat het chemisch stabiel is in waterige oplossing en in het celmembraan. IBS-wetenschappers ontdekten dat PB-1A zichzelf van nature in het celmembraan invoegt, is functioneel als een ionkanaal, en niet giftig voor cellen.
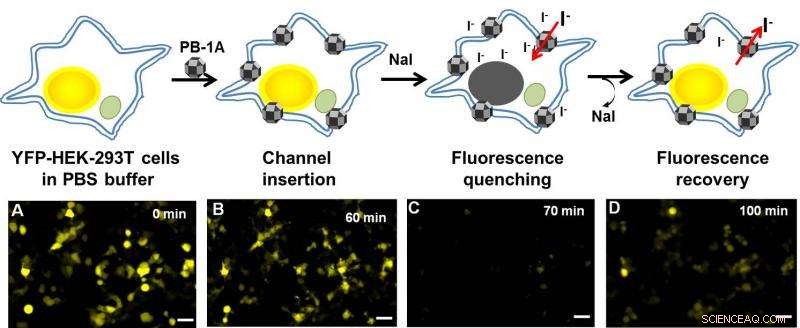
Jodide (I-) komt binnen en verlaat het via de synthetische PB-1A-kanalen in het celmembraan. Cellen worden behandeld met jodide-gevoelige gele fluorescerende eiwitten (YFP-HEK-293T-cellen) die alleen fluorescerend zijn in afwezigheid van I-(A). IBS-wetenschappers merkten op dat de toevoeging van PB-1A-kanalen niet interfereerde met de fluorescentie (B), maar een uur later toen ze I- (als natriumjodide, NaI), de fluorescentie werd gedoofd (C). De NaI-oplossing werd vervolgens verwijderd, en de fluorescentie verscheen weer na 30 minuten, wat aangeeft dat I- uit de cel diffundeerde via de PB-1A-kanalen (D). Krediet:Instituut voor Basiswetenschappen
Het team merkte op dat verschillende soorten negatief geladen ionen door PB-1A kunnen gaan, maar sommigen kunnen het beter dan anderen. Bijvoorbeeld:jodide-overdracht ongeveer 60 keer efficiënter dan chloride, het meest voorkomende biologisch negatief geladen ion, dat is twee keer selectiever dan eerder gerapporteerde kanalen. Het team merkte op dat verschillende soorten negatief geladen ionen door PB-1A kunnen gaan, maar sommigen kunnen het beter dan anderen. Bijvoorbeeld:jodide transporteert ongeveer 60 keer efficiënter dan chloride, het meest voorkomende biologisch negatief geladen ion, die twee keer selectiever is dan eerder gerapporteerde kanalen. Dit verschil in efficiëntie houdt verband met de watermoleculen die de ionen omringen en de energie die nodig is om ze eruit te trekken, d.w.z. het is gemakkelijker voor jodide om deze watermoleculen te verwijderen als het door het kanaal gaat, wat de doorgang vergemakkelijkt.
Het ontwerpen van kanalen met een hoge selectiviteit voor specifieke ionen is geen triviale taak. "We zijn enthousiast over deze bevindingen, omdat in vergelijking met studies over chloridekanalen en kanalen die positief geladen ionen transporteren, Jodide-selectieve kunstmatige kanalen zijn de afgelopen tien jaar zelden gemeld. Bovendien, kanalen die de functies van NIS nabootsen zijn erg interessant, omdat ze mogelijk schildklier- en niet-schildklierkanker kunnen behandelen, " wijst Dr. ROH Joon Ho aan, een van de corresponderende auteurs van deze studie.
 Onderzoekers ontdekken heetste lava die in de afgelopen 2,5 miljard jaar is uitgebarsten
Onderzoekers ontdekken heetste lava die in de afgelopen 2,5 miljard jaar is uitgebarsten Aanzienlijke uitstoot van kooldioxide uit noordelijke veengebieden die zijn ontwaterd voor de teelt van gewassen
Aanzienlijke uitstoot van kooldioxide uit noordelijke veengebieden die zijn ontwaterd voor de teelt van gewassen Decadale klimaatvariabiliteit in de tropische Stille Oceaan
Decadale klimaatvariabiliteit in de tropische Stille Oceaan Stadia van de Mongo Seed
Stadia van de Mongo Seed NASA-beelden tonen ongeorganiseerde tropische depressie 8E
NASA-beelden tonen ongeorganiseerde tropische depressie 8E
Hoofdlijnen
- Licht schijnen op het sociale leven van virussen
- Het publiek is minder bang voor haaien als ze hun gedrag begrijpen
- Wat is het verschil tussen een protist en een menselijke huidcel?
- Hoe beïnvloedt het hebben van twee van elk soort chromosoom de genen die een persoon heeft?
- Hoe gedraag je je in een dierentuin - volgens de wetenschap
- Sneeuwuilaantallen veel lager dan ooit gedacht
- Van stroper tot boswachter:de Siberische tijgers van China redden
- Begrazingsbeheer voor vee compatibel met nestelende saliekorhoen
- Griezelige bescherming:bedreigde diersoorten redden boven onze dode lichamen
- Moleculen maken die fonkelen
- Hoogrenderende katalysator verbetert de elektrische reductieprestaties van kooldioxide

- Nieuwe software brengt cryo-EM-kaarten met een lagere resolutie in beeld

- Warmte en licht creëren nieuwe biocompatibele microdeeltjes
- Nieuw elektrisch geactiveerd materiaal kan braillelezers verbeteren

 Fatale fouten in de prijs van een leven van de Britse regering
Fatale fouten in de prijs van een leven van de Britse regering Natuurkundigen rekken diamant uit met behulp van een elektrisch veld
Natuurkundigen rekken diamant uit met behulp van een elektrisch veld De meest gezwollen super-Neptunus heeft een wolkenvrije atmosfeer, nieuwe studie vondsten
De meest gezwollen super-Neptunus heeft een wolkenvrije atmosfeer, nieuwe studie vondsten Hoe het percentage te berekenen Overvloed van een isotoop
Hoe het percentage te berekenen Overvloed van een isotoop Detectorarray demonstreert nieuwe microgolfuitlezing
Detectorarray demonstreert nieuwe microgolfuitlezing Cyberspace is het volgende front in het conflict tussen Iran en de VS - en particuliere bedrijven kunnen de dupe worden
Cyberspace is het volgende front in het conflict tussen Iran en de VS - en particuliere bedrijven kunnen de dupe worden Zeldzame foto's van vroege NASA-astronauten worden geveild
Zeldzame foto's van vroege NASA-astronauten worden geveild Dangerous Bugs & Spiders in Tennessee
Dangerous Bugs & Spiders in Tennessee
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway | French |

-
Wetenschap © https://nl.scienceaq.com

