
Wetenschap
Waarom worden de lanthaniden en sctiniden aan de onderkant van de periodieke tabel geplaatst?
1. Ruimtebeperkingen:
* Het periodiek systeem is georganiseerd door het atoomnummer en de elektronenconfiguratie te vergroten.
* De lanthaniden en actiniden hebben zeer vergelijkbare chemische eigenschappen vanwege hun F-blok elektronenconfiguratie.
* Het opnemen van ze in het hoofdlichaam van de tafel zou het te breed en onhandig maken, waardoor de visuele organisatie wordt verstoord.
2. Periodiciteit handhaven:
* Door ze onderaan te plaatsen, kunnen de hoofdlichaam van de tabel de periodiciteit van elementen weerspiegelen in termen van hun chemische eigenschappen en valentie -elektronenconfiguraties.
* Deze opstelling houdt elementen met vergelijkbare chemische eigenschappen in dezelfde verticale kolommen (groepen).
3. Visuele duidelijkheid:
* Deze opstelling benadrukt de unieke aard van de lanthaniden en actiniden als afzonderlijke series met verschillende eigenschappen.
4. Historische redenen:
* Vroege versies van het periodiek systeem bevatten deze elementen niet.
* Terwijl ze werden ontdekt, kwam de plaatsing onderaan naar voren als de meest logische oplossing om de structuur en organisatie van de tabel te behouden.
Samenvattend: Het plaatsen van de lanthaniden en actiniden onderaan de periodiek systeem is een praktische en logische oplossing die:
* Bewaar de organisatie van de tabel op basis van elektronenconfiguratie.
* Handhaaft de periodieke trends van chemische eigenschappen.
* Biedt visuele duidelijkheid.
* Weerspiegelt de historische ontwikkeling van de tabel.
 Sterke coördinatie-interactie geïdentificeerd als gunstig voor het bevorderen van dehydrogenering van ethanol
Sterke coördinatie-interactie geïdentificeerd als gunstig voor het bevorderen van dehydrogenering van ethanol  Intensivering van de productie van hoogwaardige verbindingen uit industrieel afval
Intensivering van de productie van hoogwaardige verbindingen uit industrieel afval  LAN is de formule voor welke ionische verbinding?
LAN is de formule voor welke ionische verbinding?  Wat is een niet -voorbeeld van chemische vergelijking?
Wat is een niet -voorbeeld van chemische vergelijking?  Wat zijn het juiste paar complementaire stikstofbases in DNA?
Wat zijn het juiste paar complementaire stikstofbases in DNA?
 Hoe is wetenschapper op zoek naar een buitenaards leven?
Hoe is wetenschapper op zoek naar een buitenaards leven?  Hoe veroorzaken tyfoons kustalgenbloei?
Hoe veroorzaken tyfoons kustalgenbloei? Sterke aanwijzingen voor ververst grondwater voor de kust van de Maltese eilanden
Sterke aanwijzingen voor ververst grondwater voor de kust van de Maltese eilanden Hoe ademt een rivier? Het antwoord zou kunnen leiden tot een beter begrip van de mondiale koolstofcyclus
Hoe ademt een rivier? Het antwoord zou kunnen leiden tot een beter begrip van de mondiale koolstofcyclus  Welke kwaliteiten zijn een goede wetenschappelijke vraag?
Welke kwaliteiten zijn een goede wetenschappelijke vraag?
Hoofdlijnen
- Wat doen de lysosomen voor een plantencel?
- Wat betekent het woord gezin in de wetenschap?
- Hoe MRNA van een cel te isoleren
- Welke microscoop wordt gebruikt voor het observeren van gistmitochondriën?
- Welke veel voorkomende aandoening wordt veroorzaakt door de aanwezigheid van drie kopieën chromosoom 21?
- Welke functionele groep wordt altijd aangetroffen in aminozuren?
- Hoe technologie ons in staat stelt de geheimen van de Amazone-biodiversiteit te onthullen
- Hoe verschillen de reproductieve structuren van een typisch-gymnosperm van elkaar?
- Onderzoekers klonen half-rankloze genlocus in erwtenmutantafila
- Wetenschappers bedenken diervrije testen van dodelijke neurotoxines

- Nieuwe techniek brengt de studie van moleculaire configuratie in het microscopische domein

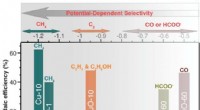
- Selectieve katalysatoren voor recycling van kooldioxide
- Hoe beïnvloeden stromingskrachten van geladen oppervlakken/deeltjes en oppervlakteactieve stoffen in vloeistoffen?

- Ongrijpbare verbindingen van broeikasgas geïsoleerd

 Wat is een alledaags object dat een vorm heeft die vergelijkbaar is met de aarde?
Wat is een alledaags object dat een vorm heeft die vergelijkbaar is met de aarde?  Laboratoriumtests tonen aan dat molecuul celdood in tumoren lijkt te stimuleren, ontsteking
Laboratoriumtests tonen aan dat molecuul celdood in tumoren lijkt te stimuleren, ontsteking Hoe zijn vaste en gasvloeistof hetzelfde?
Hoe zijn vaste en gasvloeistof hetzelfde?  Rechtbanken AT&T-Time Warner-uitspraak duidelijk onjuist:Amerikaanse regering
Rechtbanken AT&T-Time Warner-uitspraak duidelijk onjuist:Amerikaanse regering Recordbrekend zwak satellietstelsel van de Melkweg ontdekt
Recordbrekend zwak satellietstelsel van de Melkweg ontdekt Nieuwe methode gebruikt om supernovarest DEM L71 . te onderzoeken
Nieuwe methode gebruikt om supernovarest DEM L71 . te onderzoeken Het partijdige brein:cognitieve studie suggereert dat mensen links en rechts meer op elkaar lijken dan ze denken
Het partijdige brein:cognitieve studie suggereert dat mensen links en rechts meer op elkaar lijken dan ze denken Wetenschappers onthullen een nauw verband tussen luchttemperatuur en het gebied van Antarctische polynyas
Wetenschappers onthullen een nauw verband tussen luchttemperatuur en het gebied van Antarctische polynyas
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

