
Wetenschap
Zijn 0,5 mol NaOH- en 0,5 m -oplossing hetzelfde?
* Moles vertegenwoordigen het bedrag van inhoud. 0,5 mol NaOH betekent dat u 0,5 * Avogadro's aantal * NaOH -moleculen hebt.
* molariteit (m) vertegenwoordigt de concentratie van een oplossing. Een 0,5 m oplossing van NaOH betekent dat u 0,5 mol NaOH hebt opgelost in 1 liter oplossing.
Denk er op deze manier aan:
* Moles zijn als het aantal appels je hebt.
* molariteit is als de -dichtheid van appels in een mand.
U kunt 0,5 mol NaOH hebben in verschillende volumes van oplossing, wat resulteert in verschillende molariteiten.
Bijvoorbeeld:
* 0,5 mol NaOH opgelost in 1 liter water zou een oplossing van 0,5 M zijn.
* 0,5 mol NaOH opgelost in 0,5 liter water zou een oplossing van 1 m zijn.
Conclusie, Mollen en molariteit zijn gerelateerde maar verschillende concepten. Mol meten de hoeveelheid stof, terwijl molariteit de concentratie van die stof in een oplossing meet.
 What Dissolves Oil?
What Dissolves Oil?  Hoe zou u het hoofd chloride scheiden van het mengsel van en zilveren chloride?
Hoe zou u het hoofd chloride scheiden van het mengsel van en zilveren chloride?  Geïnspireerd door fotosynthese, wetenschappers dubbele reactie kwantumefficiëntie
Geïnspireerd door fotosynthese, wetenschappers dubbele reactie kwantumefficiëntie Hoe gebruik je het wetenschappelijke woord atoom in een zin?
Hoe gebruik je het wetenschappelijke woord atoom in een zin?  Een laserfocus op het vinden van betere manieren om hernieuwbare brandstoffen te maken
Een laserfocus op het vinden van betere manieren om hernieuwbare brandstoffen te maken
 Recordhoeveelheid hernieuwbare energiecapaciteit toegevoegd in 2016:UN
Recordhoeveelheid hernieuwbare energiecapaciteit toegevoegd in 2016:UN Het klimaat van China in 2019:warmer en natter, maar minder verlies
Het klimaat van China in 2019:warmer en natter, maar minder verlies Een verbod op oliepalm blokkeert goede praktijken
Een verbod op oliepalm blokkeert goede praktijken Wetenschappers porren een gat in de leeftijd van bomen
Wetenschappers porren een gat in de leeftijd van bomen Everest:ik reisde de doodszone in om 's werelds hoogste weerstation te installeren
Everest:ik reisde de doodszone in om 's werelds hoogste weerstation te installeren
Hoofdlijnen
- Wat is differentiële evolutie?
- Wat moet een organisme stabiele interne omstandigheden behouden?
- Wat is de reden dat plantencellen een extra dikke buitenste bedekking hebben en die worden genoemd?
- Testen hoe goed chemische cellen werken, zou een antwoord kunnen bieden op het herkennen van leven
- Welk enzym verteert eiwit?
- Wanneer wordt een foetus twee cellen?
- Waarschijnlijke voorouder van alle geïdentificeerde moderne hoefdieren
- Sanctuary-chimpansees vertonen hoge percentages resistente stafylokok
- Welke functie heeft emb-agar?
- Kunstmatige membraanbindende eiwitten om stamcellen naar het myocardium te leiden
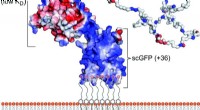
- Voor het eerst het verschil in structurele dynamiek van 1 nm enkelvoudige moleculen bij kamertemperatuur waarnemen
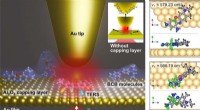
- Een nieuw soort lijm om polyethyleen te verlijmen
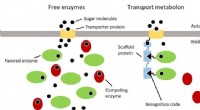
- Efficiënter omgaan met grondstoffen met behulp van moleculaire transportbanden
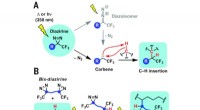
- Nieuw licht op het maken van tweedimensionale polymeren

 Hoe beweegt een raket zich en verandert van richting in de ruimte?
Hoe beweegt een raket zich en verandert van richting in de ruimte?  AI-model beveelt gepersonaliseerde lettertypen aan om digitaal lezen en toegankelijkheid te verbeteren
AI-model beveelt gepersonaliseerde lettertypen aan om digitaal lezen en toegankelijkheid te verbeteren Zijn er beroemde vulkanen op Cyprus?
Zijn er beroemde vulkanen op Cyprus?  Hoe gedragen watermoleculen zich?
Hoe gedragen watermoleculen zich?  Giftige algen nemen toe in Lake Okeechobee in Florida
Giftige algen nemen toe in Lake Okeechobee in Florida Sociale normen beïnvloeden de bereidheid om het klimaat te beschermen
Sociale normen beïnvloeden de bereidheid om het klimaat te beschermen Wat is de slimste ster in Ursa Minor Constellation?
Wat is de slimste ster in Ursa Minor Constellation?  Welke kracht veroorzaakt versnelling?
Welke kracht veroorzaakt versnelling?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

