
Wetenschap
Hoe gedragen watermoleculen zich?
1. Polariteit:
* gebogen vorm: Het molecuul heeft een gebogen vorm vanwege de twee eenzame paren elektronen op het zuurstofatoom, waardoor het molecuul polair is.
* ongelijke laadverdeling: Het zuurstofatoom is elektronegatiefer, wat betekent dat het elektronen sterker aantrekt dan de waterstofatomen. Dit creëert een gedeeltelijke negatieve lading aan de zuurstofzijde en gedeeltelijke positieve ladingen aan de waterstofzijden.
2. Waterstofbinding:
* Sterke attracties: De gedeeltelijke positieve lading op het waterstofatoom van één watermolecuul wordt aangetrokken door de gedeeltelijke negatieve lading op het zuurstofatoom van een ander watermolecuul. Dit vormt een sterke intermoleculaire binding die een waterstofbinding wordt genoemd.
* Hoge cohesie en hechting: Waterstofbindingen zijn verantwoordelijk voor de hoge cohesie van water (aantrekkingskracht tussen watermoleculen) en hechting (aantrekkingskracht op andere oppervlakken). Dit verklaart het vermogen van water om smalle buizen op te reizen (capillaire actie) en de oppervlaktespanning.
3. Dynamisch en flexibel:
* constante beweging: Watermoleculen bewegen, roteren en trillen constant, breken en hervormen waterstofbindingen. Deze dynamiek verklaart het vermogen van water om een breed scala aan stoffen op te lossen en de relatief hoge warmtecapaciteit ervan (vermogen om warmte te absorberen zonder significante temperatuurverandering).
4. Staten van materie:
* vloeibare status: De waterstofbindingen in water zijn sterk genoeg om de moleculen dicht bij elkaar te houden, waardoor een vloeibare toestand ontstaat.
* vaste toestand (ijs): Wanneer water bevriest, worden de moleculen minder mobiel en vormen ze een rigide, kristallijne structuur met een lagere dichtheid dan vloeibaar water. Dit is de reden waarom ijs zweeft.
* Gaseous State (damp): Bij hoge temperaturen hebben de moleculen voldoende energie om de waterstofbruggen te breken en te ontsnappen in de gasfase.
5. Eigenschappen beïnvloed door gedrag:
* Hoog kookpunt: Water heeft een hoog kookpunt vanwege de sterke waterstofbruggen tussen moleculen.
* Universeel oplosmiddel: Met waterpolariteit en waterstofbinding kan het veel polaire en ionische stoffen oplossen.
* Hoge warmtecapaciteit: Water kan veel warmte absorberen voordat de temperatuur aanzienlijk verandert, waardoor het een belangrijke temperatuurregelaar is.
* Oppervlaktespanning: Wateroppervlakspanning wordt veroorzaakt door de sterke samenhangende krachten tussen moleculen, waardoor het zich gedraagt als een dun elastisch vel.
Samenvattend resulteert het gedrag van watermoleculen, aangedreven door hun polariteit en waterstofbinding, in unieke eigenschappen die cruciaal zijn voor het leven op aarde. Ze laten water een uitstekend oplosmiddel zijn, de temperaturen reguleren en het leven ondersteunen door zijn opmerkelijke eigenschappen.
 Atlantisch orkaanseizoen kan extreem actief zijn:NOAA
Atlantisch orkaanseizoen kan extreem actief zijn:NOAA De analogiemethode toepassen om de voorspelling van sterke convectie te verbeteren
De analogiemethode toepassen om de voorspelling van sterke convectie te verbeteren Een globale kijk op organische koolstof aan de oppervlakte
Een globale kijk op organische koolstof aan de oppervlakte Analyse van vogelsoorten laat zien hoe vleugels zich aanpasten aan hun omgeving en gedrag
Analyse van vogelsoorten laat zien hoe vleugels zich aanpasten aan hun omgeving en gedrag  NASA-infraroodbeelden onthullen windschering die de sterkste stormen van Marie verdringt
NASA-infraroodbeelden onthullen windschering die de sterkste stormen van Marie verdringt
Hoofdlijnen
- Wat zijn de naam en site van een laboratoriumapparatuur?
- Welke lichaamssystemen zijn betrokken bij de ademhaling?
- Wat scheidt de cel van zijn omgeving en selecteert wat kan invoeren?
- Welk enzym is betrokken bij RNA -verlenging?
- Een ingenieursgids voor het embryo
- What Is Crossing Over in Genetics?
- Onderzoek met bacteriën brengt wetenschappers een stap dichter bij het maken van kunstmatige cellen met levensechte functionaliteit
- Colombia,
- Wanneer kan een wetenschapper model gebruiken als onderzoeksmethode?
- Hoe zuurstof de kern van belangrijke enzymen vernietigt

- Studie volgt innerlijke werking van de hersenen met nieuwe biosensor

- Je gelooft het maar:caloriearme spread voornamelijk gemaakt van water

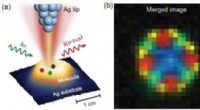
- Raman-picoscopie scannen:een nieuwe methode voor het bepalen van de moleculaire chemische structuur
- Composteerbaar bioleer biedt duurzame oplossingen voor de kledingindustrie en daarbuiten

 Hoe helpt de celwand van een bewaker en chloroplasten zich te helpen zijn functie uit te voeren?
Hoe helpt de celwand van een bewaker en chloroplasten zich te helpen zijn functie uit te voeren?  Facebook kan anti-vaxx-berichten verbergen nadat het wordt beschuldigd van het verspreiden van nepnieuws over gezondheid
Facebook kan anti-vaxx-berichten verbergen nadat het wordt beschuldigd van het verspreiden van nepnieuws over gezondheid De industrie smeren, de natuurlijke manier
De industrie smeren, de natuurlijke manier Nieuwe ontdekking om de ontwikkeling van zouttolerante wijnstokken te versnellen
Nieuwe ontdekking om de ontwikkeling van zouttolerante wijnstokken te versnellen Brandstoflekken dreigen de lancering van nieuwe NASA-maanraket te vertragen (update)
Brandstoflekken dreigen de lancering van nieuwe NASA-maanraket te vertragen (update) Gesteente bemonsterd door NASA's Perseverance belichaamt waarom de rover naar Mars kwam
Gesteente bemonsterd door NASA's Perseverance belichaamt waarom de rover naar Mars kwam  Fotonica:grafeen versterkt on-chip lichtdetectoren
Fotonica:grafeen versterkt on-chip lichtdetectoren Op welke twee variabelen is versnelling afhankelijk van en wat de relatie tussen deze versnelling?
Op welke twee variabelen is versnelling afhankelijk van en wat de relatie tussen deze versnelling?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

