
Wetenschap
Waar zijn waterstofionen in een waterige oplossing altijd mee aan?
Dit is waarom:
* waterstofionen zijn zeer reactief: Ze hebben een sterke neiging om een elektron te krijgen om neutraal te worden.
* Watermoleculen zijn polair: Ze hebben een gedeeltelijke positieve lading op de waterstofatomen en een gedeeltelijke negatieve lading op het zuurstofatoom.
* Hydronium -ionenvorming: De positieve lading op het waterstofion trekt het enige paar elektronen aan op het zuurstofatoom van een watermolecuul, waardoor een covalente binding wordt gevormd. Dit resulteert in een hydroniumion (H3O+).
Hoewel we vaak H+ schrijven om waterstofionen in oplossing weer te geven, is het belangrijk om te onthouden dat ze bestaan als hydroniumionen in aanwezigheid van water.
 Wat is de pH van citroenzuur?
Wat is de pH van citroenzuur?  De sleutel tot verbeterde efficiëntie van groene technologie gevonden in eenvoudige zuurbehandeling
De sleutel tot verbeterde efficiëntie van groene technologie gevonden in eenvoudige zuurbehandeling Wat is het verschil tussen ISBN 13 & ISBN 10?
Wat is het verschil tussen ISBN 13 & ISBN 10?  Een leerling moet 15 gram zout afmeten. Het zout wordt geleverd in potten van 500 g. wat moet eerst doen?
Een leerling moet 15 gram zout afmeten. Het zout wordt geleverd in potten van 500 g. wat moet eerst doen?  Hoeveel chemicaliën eet je?
Hoeveel chemicaliën eet je?
Hoofdlijnen
- Hoe vaccins werken
- Om de effecten van langere, hetere zomers te bestuderen, slepen ecologen 5000 kilo zand de berg op
- Team onderzoekt hoe egoïstische genen mannelijke onvruchtbaarheid veroorzaken bij bloeiende planten
- Waarom het laten ontsnappen van zalm gunstig zou kunnen zijn voor beren en vissers
- Nieuw model helpt verklaren hoe voorzieningen ziekten in het wild bevorderen of verminderen
- Wat zijn protist die lijken op planten die dieren of schimmels worden genoemd?
- Wat zijn drie verschillende metingen die populaties beschrijven?
- De nadelen van Western Blotting
- Wat is een organisme in actie en verandert het gedrag dat optreedt als gevolg van een stimulus?
- snel, flexibele wateranalyse zorgt voor opschudding in de industrie

- Molecuul valt coronavirus op een nieuwe manier aan

- Machine learning-benadering kan helpen bij het ontwerpen van industriële processen voor de productie van geneesmiddelen

- Verven en lakken op basis van aardappelzetmeel

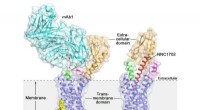
- Glucagon-receptorstructuur biedt nieuwe mogelijkheden voor het ontdekken van geneesmiddelen voor type 2 diabetes
 Welk gas ontstaat uit ontbindingsafvalmateriaal op een stortplaats?
Welk gas ontstaat uit ontbindingsafvalmateriaal op een stortplaats?  Wordt de vraag naar astronomen en andere ruimte -experts toeneemt?
Wordt de vraag naar astronomen en andere ruimte -experts toeneemt?  Zijn wetten alleen aangevraagd voor de 6 planeten die in zijn tijd bekend zijn?
Zijn wetten alleen aangevraagd voor de 6 planeten die in zijn tijd bekend zijn?  Rechtbank oordeelt dat Trump EPA onwettig gevaarlijke chemicaliën negeerde
Rechtbank oordeelt dat Trump EPA onwettig gevaarlijke chemicaliën negeerde Zwart georiënteerde films kunnen zeer winstgevend zijn wanneer ze voor alle doelgroepen op de markt worden gebracht, studie vondsten
Zwart georiënteerde films kunnen zeer winstgevend zijn wanneer ze voor alle doelgroepen op de markt worden gebracht, studie vondsten Wat is wetenschappelijke notatie voor 420?
Wat is wetenschappelijke notatie voor 420?  Waarom propaan wordt verbrandt Water
Waarom propaan wordt verbrandt Water Ultrasnelle elektronenmetingen maken in meerdere richtingen om de geheimen van de aurora te onthullen
Ultrasnelle elektronenmetingen maken in meerdere richtingen om de geheimen van de aurora te onthullen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

