
Wetenschap
Wat is de pH van citroenzuur?
Dit is waarom:
* citroenzuur is een zwak zuur. Dit betekent dat het niet volledig in water wordt gescheiden en slechts een deel van zijn waterstofionen (H+) vrijgeeft.
* De concentratie citroenzuur bepaalt de concentratie van H+ ionen. Hogere concentraties citroenzuur zullen leiden tot meer afgegeven H+ -ionen, waardoor de oplossing zuurder wordt (lagere pH).
* De pH van een citroenzuuroplossing kan worden berekend met behulp van een pH -formule. Deze formule houdt rekening met de concentratie citroenzuur en zijn dissociatieconstante (KA).
Dus in plaats van een enkele pH -waarde, praten we over het pH -bereik van citroenzuuroplossingen. Een citroenzuuroplossing van 1% heeft bijvoorbeeld een pH rond 2,2, terwijl een oplossing van 0,1% een pH rond 2,8 heeft.
In het algemeen zijn citroenzuuroplossingen zuur, met pH -waarden variërend van 2 tot 3.
 Nieuw, goedkoop alternatief voor ethyleenproductie
Nieuw, goedkoop alternatief voor ethyleenproductie Waarom zouden zoutzuur en natriumhydroxide worden gebruikt bij neutralisatie in plaats van andere zuren en alkaliën?
Waarom zouden zoutzuur en natriumhydroxide worden gebruikt bij neutralisatie in plaats van andere zuren en alkaliën?  Wat is de opgeloste stof en het oplosmiddel in rozenwater?
Wat is de opgeloste stof en het oplosmiddel in rozenwater?  Ingenieurs krijgen grip op gladde oppervlakteactieve stoffen
Ingenieurs krijgen grip op gladde oppervlakteactieve stoffen Maakt THC een deel van mijn chemische make -up?
Maakt THC een deel van mijn chemische make -up?
 Menselijk afvalwater dat schadelijke algen voedt voor de kust van Zuid-Californië
Menselijk afvalwater dat schadelijke algen voedt voor de kust van Zuid-Californië Air France compenseert de dagelijkse CO2-uitstoot tegen volgend jaar
Air France compenseert de dagelijkse CO2-uitstoot tegen volgend jaar NASA's Aqua-satelliet ziet tropische depressie Calvin doordrenkt Mexico
NASA's Aqua-satelliet ziet tropische depressie Calvin doordrenkt Mexico 'S Werelds grootste steden zijn afhankelijk van verdampt water uit de omliggende landen
'S Werelds grootste steden zijn afhankelijk van verdampt water uit de omliggende landen Voor sommige stedelijke gebieden is een opwarmend klimaat is slechts de helft van de bedreiging
Voor sommige stedelijke gebieden is een opwarmend klimaat is slechts de helft van de bedreiging
Hoofdlijnen
- Welke organen van het lichaam zijn het meest waarschijnlijk getroffen door adr?
- Wat zou een cel met 44 chromosomen eindigen?
- Waarom leven vrouwen langer dan mannen?
- Produceren planten als ze geen zuurstof hebben?
- Waarom zijn zebramosselen zo plakkerig? Onderzoek kan leiden tot nieuwe industriële coatings, medische lijmen
- Bacteriën zijn leden van welke koninkrijken?
- Wanneer een cel zich voortplant, wat gebeurt er met zijn DNA?
- Hoe een beter begrip van het gedrag van hermelijnen de bestrijding van roofdieren in Aotearoa zal helpen
- Wat betekent scheiden in de menselijke biologie?
- Verslavende notenderivaten kunnen rokers helpen de nicotinegewoonte te doorbreken

- Onderzoekers vinden een chemische oplossing om digitale gegevensopslag te verkleinen

- Nieuwe techniek zet ammoniak naadloos om in groene waterstof

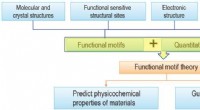
- De cruciale rol van functionele motieven—microstructurele eenheden die materiële functies bepalen—in materiaalonderzoek
- Verlenging van de levensduur van polymeerelektrolyt-brandstofcellen met een nanogedispergeerd ionomeer

 Beschermde mariene gebieden sluiten niet aan bij de kernhabitats van zeldzame trekvissen, zo blijkt uit nieuw onderzoek
Beschermde mariene gebieden sluiten niet aan bij de kernhabitats van zeldzame trekvissen, zo blijkt uit nieuw onderzoek  Subtielere vormen van intimidatie tasten het legitimiteitsgevoel van vrouwen in de natuurkunde aan
Subtielere vormen van intimidatie tasten het legitimiteitsgevoel van vrouwen in de natuurkunde aan Nieuwe algoritmen geven digitale afbeeldingen realistischere kleuren
Nieuwe algoritmen geven digitale afbeeldingen realistischere kleuren Streaming tv-oorlog komt op gang met Apple, Disney lanceert
Streaming tv-oorlog komt op gang met Apple, Disney lanceert Wat wordt door geologen gebruikt om te leren over het interieur van de aarde?
Wat wordt door geologen gebruikt om te leren over het interieur van de aarde?  Van moestuinieren tot op-shopping, migranten zijn de stille milieuactivisten
Van moestuinieren tot op-shopping, migranten zijn de stille milieuactivisten Paleontoloog gelooft dat Mosasaurus uit het Krijt zich misschien heeft gespecialiseerd in vis
Paleontoloog gelooft dat Mosasaurus uit het Krijt zich misschien heeft gespecialiseerd in vis Wat is de oxidatiereactie voor koolmonoxide en zuurstof?
Wat is de oxidatiereactie voor koolmonoxide en zuurstof?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

