
Wetenschap
Stoffen met alleenstaande paren op Central Atom?
Wat zijn eenzame paren?
* Eenzame paren zijn paren elektronen in de buitenste schaal van een atoom die niet betrokken zijn bij de binding.
* Ze dragen bij aan de vorm van het molecuul en beïnvloeden de polariteit ervan.
Moleculen identificeren met eenzame paren:
1. Lewis -structuren: Begin met het tekenen van de Lewis -structuur van het molecuul. Dit toont u de opstelling van binding en niet-bindende elektronen.
2. Valence -elektronen: Overweeg de valentie -elektronen van het centrale atoom.
3. binding: Bepaal hoeveel elektronen het centrale atoom gebruikt voor binding.
4. eenzame paren: Trek het aantal bindingselektronen af van de totale valentie -elektronen. De resterende elektronen zijn eenzame paren.
Voorbeelden:
* water (h₂o): Zuurstof heeft 6 valentie -elektronen. Het vormt twee enkele bindingen met waterstofatomen (2 gebruikte elektronen). Dit laat 4 elektronen achter en vormt twee eenzame paren op het zuurstofatoom.
* ammoniak (NH₃): Stikstof heeft 5 valentie -elektronen. Het vormt drie enkele bindingen met waterstofatomen (3 gebruikte elektronen). Dit laat 2 elektronen achter en vormt één eenzaam paar op het stikstofatoom.
* methaan (ch₄): Koolstof heeft 4 valentie -elektronen. Het vormt vier enkele bindingen met waterstofatomen (4 gebruikte elektronen). Er zijn geen resterende elektronen voor alleenstaande paren.
Gemeenschappelijke moleculen met enige paren op het centrale atoom:
* Groep 16 (zuurstofgroep): Water (H₂o), waterstofsulfide (H₂s), zwaveldioxide (SO₂)
* Groep 15 (stikstofgroep): Ammoniak (NH₃), fosfine (pH₃), stikstof trifluoride (NF₃)
* Groep 14 (koolstofgroep): Zwavel hexafluoride (SF₆)
Opmerking: Moleculen met alleenstaande paren op het centrale atoom vertonen vaak:
* polariteit: Eenzame paren dragen bij aan een ongelijke verdeling van elektronendichtheid, waardoor het molecuul polair is.
* Vorm: Eenzame paren kunnen de moleculaire geometrie beïnvloeden, wat vaak leidt tot gebogen of piramidevormen.
Laat het me weten als je meer voorbeelden of uitleg wilt over specifieke moleculen!
 Een gas bij dezelfde temperatuur als vloeibare toestand?
Een gas bij dezelfde temperatuur als vloeibare toestand?  Lost koffie op in water een fysische of chemische verandering?
Lost koffie op in water een fysische of chemische verandering?  Hoe de dikke darm prioriteit geeft aan gasontgifting boven energieverbruik?
Hoe de dikke darm prioriteit geeft aan gasontgifting boven energieverbruik? Unieke dendritische kleverige deeltjes gevormd door het benutten van vloeibare chaos
Unieke dendritische kleverige deeltjes gevormd door het benutten van vloeibare chaos Optische eigenschappen van polyethyleen
Optische eigenschappen van polyethyleen
Hoofdlijnen
- Indringende vraag:Waarom overleefden zoogdieren het 'K/T-uitsterven'?
- Wat zijn de gameten van planten?
- Nieuwe studie werpt licht op hoe intracellulaire pathogenen het immuunsysteem activeren
- Een muis of een olifant:welke soort bestrijdt infecties effectiever?
- Waar voeren wetenschappers hun werk uit?
- rRNA: Wat is het?
- Schimmelparing:volgend wapen tegen maïsaflatoxine?
- Grootschalig scherm laat zien hoe talloze signaalroutes elkaar kruisen in het primaire eiwitverwerkingscentrum van de cel
- Worden virussen als levend of niet-levend beschouwd?
- Herhalingssleutel tot zelfgenezing, flexibele medische hulpmiddelen

- Slimme magnetische zachte materialen om kunstmatige spieren en therapeutische robots te ontwikkelen

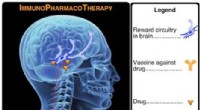
- Onderzoekers vinden een manier om farmacoterrorisme te bestrijden
- Op ijzer gebaseerde katalysatoren ontdekt in door licht aangedreven kooldioxidehydrogenering

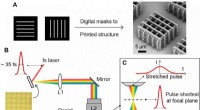
- Nieuwe techniek verhoogt 3D-printsnelheid met 1, 000 tot 10, 000 keer
 Boeings Starliner-capsule maakt lanceringsdebuut, maar raakt addertje onder het gras (update)
Boeings Starliner-capsule maakt lanceringsdebuut, maar raakt addertje onder het gras (update) Toronto schieten - de psychologie van verlies, angst en identiteit
Toronto schieten - de psychologie van verlies, angst en identiteit Is MLB klaar om te strijden om de volgende generatie fans?
Is MLB klaar om te strijden om de volgende generatie fans? Het is dringend nodig om na te gaan hoe mannen en vrouwen verschillend reageren op de verzuring van de oceaan
Het is dringend nodig om na te gaan hoe mannen en vrouwen verschillend reageren op de verzuring van de oceaan  Capsule met asteroïde-monsters arriveert in Japan voor onderzoek
Capsule met asteroïde-monsters arriveert in Japan voor onderzoek Wanneer school aanvoelt als scores voor gevangenistests, daalt het collegebezoek
Wanneer school aanvoelt als scores voor gevangenistests, daalt het collegebezoek  Afbeelding:SOHO's equinox zon
Afbeelding:SOHO's equinox zon Index om belangrijke systeemprocessen in ecosystemen te identificeren
Index om belangrijke systeemprocessen in ecosystemen te identificeren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

