
Wetenschap
Wat is de groepsvolgorde van alkali -metalen door reactie?
* Afnemende ionisatie -energie: Het buitenste elektron is gemakkelijker te verwijderen als u de groep afloopt omdat het elektron verder van de kern is en wordt afgeschermd door meer binnenste elektronenschalen.
* toenemende atomaire straal: De grotere omvang van de atomen verderop in de groep maakt het voor hen gemakkelijker om hun valentie -elektron te verliezen.
Hier is de volgorde van reactiviteit van alkali -metalen van minst tot meest reactief:
1. lithium (li)
2. Natrium (NA)
3. kalium (k)
4. rubidium (RB)
5. cesium (CS)
6. Francium (FR)
Belangrijke opmerking: Francium is radioactief en uiterst zeldzaam, dus de reactiviteit ervan is niet gemakkelijk waargenomen.
Voorbeelden van reactiviteit:
* lithium: Reageert langzaam met koud water.
* natrium: Reageert krachtig met koud water en produceert waterstofgas.
* kalium: Reageert heftig met koud water en ontstak het geproduceerde waterstofgas.
* rubidium en cesium: Reageer explosief met koud water.
Deze reactiviteitstrend is een belangrijk kenmerk van alkali -metalen, waardoor ze nuttig zijn in verschillende toepassingen zoals batterijen, organische chemie en geneesmiddelen.
 Nieuw onderzoek identificeert overvloedige bedreigde vissen onder waterval in San Juan River
Nieuw onderzoek identificeert overvloedige bedreigde vissen onder waterval in San Juan River USGS identificeert het grootste continue potentieel voor olie- en gasbronnen ooit
USGS identificeert het grootste continue potentieel voor olie- en gasbronnen ooit Gezondheidsrisicoalarm over waterrantsoenering in Rome
Gezondheidsrisicoalarm over waterrantsoenering in Rome Waarom zijn bomen en bossen belangrijk?
Waarom zijn bomen en bossen belangrijk?  Wat zit er in de buitenste band van een orkaan?
Wat zit er in de buitenste band van een orkaan?
Hoofdlijnen
- Wat produceren micro -organismen?
- Wat voor redenering wordt meestal gebruikt om hypothesen te vormen?
- Hoe biologen veldwerk veiliger en rechtvaardiger maken
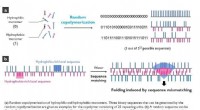
- Wetenschappers visualiseren de structuur van de belangrijkste DNA-reparatiecomponent met een bijna-atomaire resolutie
- Door hormonen uit te scheiden, zorgt de tymus ervoor dat cellen immunocompetent worden?
- Waarom gaan bacteriën naar de bodem van de bouilloncultuur?
- Wat is de volledige vorm van wetenschap?
- Wat betekent kolonies?
- Activisten willen brug over snelweg bouwen om wilde dieren veilig over te steken
- Nieuwe polymeer mesofasestructuur ontdekt
- Surrey bouwt AI om chemische verbindingen tegen veroudering te vinden

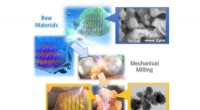
- Nieuw elektrodemateriaal ontwikkeld om de laadcapaciteit van lithiumbatterijen te vergroten
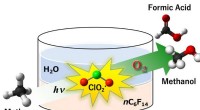
- Een radicale benadering van methaanoxidatie tot methanol
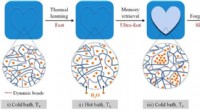
- Hydrogel bootst het menselijk brein na met het vermogen om te onthouden en te vergeten
 Ontwikkelingen voor gemengd gebruik kunnen de betaalbaarheid van woningen zelfs verminderen, sociale diversiteit
Ontwikkelingen voor gemengd gebruik kunnen de betaalbaarheid van woningen zelfs verminderen, sociale diversiteit Wat gebeurt er bij mitose die de nieuwe cel identiek DNA geeft?
Wat gebeurt er bij mitose die de nieuwe cel identiek DNA geeft?  $ 70.000 voor Zoom-lessen? De viruscrisis zorgt ervoor dat Amerikaanse studenten nijdig zijn
$ 70.000 voor Zoom-lessen? De viruscrisis zorgt ervoor dat Amerikaanse studenten nijdig zijn  Welk atoom in zijn ongebonden toestand heeft vier valentelektronen deze vormen gemakkelijk enkele dubbele en zelfs drievoudige bindingen onderling om stabiel te worden?
Welk atoom in zijn ongebonden toestand heeft vier valentelektronen deze vormen gemakkelijk enkele dubbele en zelfs drievoudige bindingen onderling om stabiel te worden?  Het destabiliserende effect van huisuitzettingen op gemeenschappen
Het destabiliserende effect van huisuitzettingen op gemeenschappen Hoeveel mol CC14 zijn aanwezig in 56G?
Hoeveel mol CC14 zijn aanwezig in 56G?  Symbiotische relaties in het Kelp Forest Ecosysteem
Symbiotische relaties in het Kelp Forest Ecosysteem Hoe kunnen we voorkomen dat de mensheid stagneert?
Hoe kunnen we voorkomen dat de mensheid stagneert?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

