
Wetenschap
Een radicale benadering van methaanoxidatie tot methanol
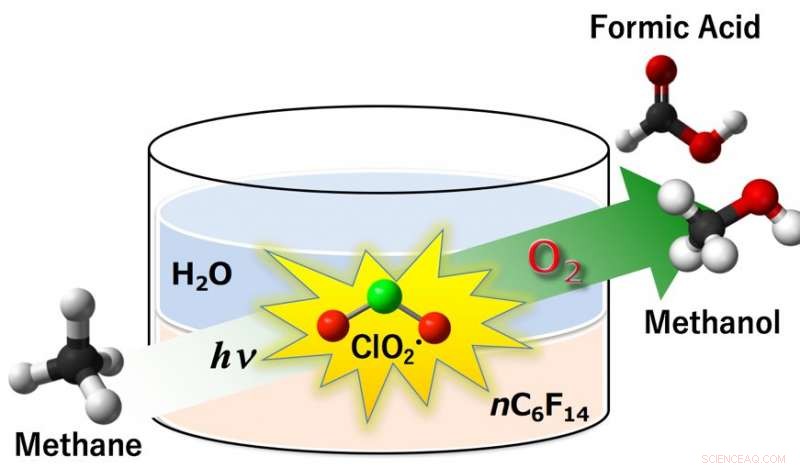
Fig.1:Chloordioxideradicaal (ClO2•) bleek te werken als een efficiënt oxidatiemiddel bij de aerobe oxygenatie van methaan tot methanol en mierenzuur onder fotobestraling. De opbrengsten van methanol en mierenzuur waren 14% en 85%, respectievelijk, met een methaanomzetting van 99% onder omgevingsomstandigheden (298 K, 1 atm) in een tweefasensysteem dat perfluorhexaan en water omvat. Krediet:Universiteit van Osaka
Vrije radicalen krijgen niet de beste pers. Echter, terwijl ze in het lichaam bekend staan als schadelijke oxidanten, deze ultrareactieve chemicaliën zijn onmisbaar in het laboratorium. Radicale reacties spelen een rol bij sleuteltechnologieën zoals verwijdering van verontreinigende stoffen en watersplitsing.
Nutsvoorzieningen, onderzoekers van de universiteit van Osaka hebben radicalen gebruikt om een broeikasgas te transformeren, methaan, tot bruikbare chemicaliën. Gedreven door licht, met dit milieuvriendelijke proces wordt een doel bereikt dat decennialang ongrijpbaar bleef.
Methaan (CH4) is verwant aan methanol en mierenzuur, die in grote hoeveelheden nodig zijn voor de chemische industrie. Bacteriën kunnen CH4 bijna moeiteloos oxideren tot methanol met behulp van natuurlijke enzymen. Dezelfde transformatie in het lab, echter, chemisch vereist hoge temperatuur, hoge druk en dure reagentia om de extreem sterke C-H-bindingen te splitsen. Zoals onlangs gemeld, het nieuwe proces gebruikt krachtige chloorradicalen om die bindingen te activeren. Hierdoor kan de reactie plaatsvinden bij kamertemperatuur, onder lamplicht, met eenvoudige zuurstof als oxidatiemiddel.
Vrije radicalen zijn chemicaliën met ongepaarde elektronen - hun ongebreidelde reactiviteit komt van de dringende behoefte aan de eenzame elektronen om partners in een ander molecuul te vinden. In het proces van Osaka, chlorietdioxide (ClO2•) wordt onder de fotobestraling geactiveerd om chloorradicalen (Cl•) en singletzuurstof te geven. De zeer reactieve radicaal, Cl•, abstraheert vervolgens een waterstofatoom van CH4 om methylradicalen te geven, CH3•, die op hun beurt reageren met zuurstof om waardevolle methanol en mierenzuur te produceren. Dit ogenschijnlijk eenvoudige proces, echter, vertrouwt op een subtiele designtwist.
"Methaanactivering door radicale soorten is eerder geprobeerd, " studie een hoofdauteur Prof. Kei Ohkubo zegt. "Echter, CH3•-tussenproducten hebben de neiging te reageren met het organische koolwaterstofoplosmiddel, waardoor de reactieve radicaaltussenproducten worden gedeactiveerd. Dit gebeurt niet in water, maar helaas lost methaan nauwelijks op in water." De onderzoekers vonden hier een nette manier omheen:twee oplosmiddelen in één systeem, één voor elke stap van het proces. De initiële ClO2•-vorming vindt plaats in een waterfase, waar natriumchloriet oplosbaar is. Vervolgens, ClO2• gaat over in een perfluorhexaan (PFH) fase, waar methaan en O2 oplossen om ermee te reageren.
"PFH is ideaal voor de tweede stap:het lost methaan op, maar reageert niet met CH3•-radicalen, " legt Ohkubo uit. "Hierdoor ontstaat ruimte voor de oxidatie van CH3•, het geven van de gewenste producten. Vervolgens, nadat methanol en mierenzuur zijn gevormd, ze passeren de grens van het oplosmiddel in de tegenovergestelde richting, in de waterfase. Hier worden ze beschermd tegen verdere oxidatie tot ongewenst CO of CO2 als broeikasgas."
Het volledige proces is indrukwekkend efficiënt, het omzetten van meer dan 99% van methaan in de doelproducten, zonder de noodzaak van hoge temperatuur of druk.
"Dit is het eerste succesvolle gebruik van zuurstof in de lucht om methaan onder omgevingsomstandigheden te oxideren, ", zegt Ohkubo. "Energie-intensieve methoden voor chemische productie moeten worden uitgefaseerd - we hebben dringend slimme oplossingen nodig om grondstoffen op een zachte, milieuvriendelijke manier. Ons onderzoek laat zien hoe dit kan voor methaan. Het tweefasenoplosmiddelconcept, waar onstabiele tussenproducten worden beschermd door een oplosmiddel zoals PFH, zou mogelijk kunnen worden uitgebreid tot de hele industrie."
Hoofdlijnen
- Wat is een Gamete?
- Studie onderzoekt de impact van leeuwen die naast giraffenpopulaties leven
- Chromosoomorganisatie komt voort uit 1-D-patronen
- Voors en tegens van Forensic Science
- Wat zijn de functies van koolhydraten in planten en dieren?
- Gist kan worden ontwikkeld om eiwitgeneesmiddelen te maken
- De soorten weefsels waarvan DNA kan worden geëxtraheerd om DNA-vingerafdrukken te maken
- Uit een grootschalig onderzoek blijkt dat veel geplande wegen in de tropen niet gebouwd mogen worden
- Exotische dieren en de jacht op goud
- Wetenschappers ontdekken nieuw veld dat invloed heeft op het stollen van metalen

- Aroma's detecteren in oude cognac

- Voedselresten krijgen een gewaagd nieuw leven

- Onderzoekers ontwikkelen een koolstofveer met hoge samendrukbaarheid en rekbaarheid

- Onderzoekers tonen aan dat zelfsteriliserende polymeren werken tegen SARS-CoV-2
 Onderzoekers ontwikkelen biologische circuitcomponenten, nieuwe microscooptechniek om ze te meten
Onderzoekers ontwikkelen biologische circuitcomponenten, nieuwe microscooptechniek om ze te meten Onderzoekers maken doorbraak in zonnecelmaterialen
Onderzoekers maken doorbraak in zonnecelmaterialen Nanobloedplaatjes verbeteren LCD- en LED-schermen
Nanobloedplaatjes verbeteren LCD- en LED-schermen Lees dit voordat u extensies in uw webbrowser installeert
Lees dit voordat u extensies in uw webbrowser installeert Waar jonge mensen naar vragen bij gegarandeerde anonimiteit
Waar jonge mensen naar vragen bij gegarandeerde anonimiteit Lokale aanjagers van versterkte Arctische opwarming
Lokale aanjagers van versterkte Arctische opwarming Effecten van zonne-energieboerderijen op het milieu
Effecten van zonne-energieboerderijen op het milieu  Eerste in de ruimte gebakken koekjes duurden twee uur in experimentele oven
Eerste in de ruimte gebakken koekjes duurden twee uur in experimentele oven
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


