
Wetenschap
Wat verklaart de observatie dat elementen van dezelfde chemische groep eigenschappen hebben?
Hier is een uitsplitsing:
* Elektronenconfiguratie: Elementen in dezelfde groep hebben hetzelfde aantal valentie -elektronen. Valentie -elektronen zijn de elektronen in het buitenste energieniveau van een atoom. Deze elektronen zijn degenen die betrokken zijn bij chemische binding, die direct het chemische gedrag van het element beïnvloeden.
* Vergelijkbare reactiviteit: Omdat ze hetzelfde aantal valentie -elektronen hebben, vormen elementen in een groep de neiging vergelijkbare chemische bindingen te vormen en op vergelijkbare manieren te reageren. Alle alkalimetalen (groep 1) hebben bijvoorbeeld één valentie -elektron, waardoor ze zeer reactief zijn en dat elektron verliezen om positieve ionen te vormen.
* Periodieke trends: Het periodiek systeem is georganiseerd op basis van terugkerende patronen in de elektronenconfiguratie. Dit leidt tot voorspelbare trends in eigenschappen, zoals atomaire straal, ionisatie -energie en elektronegativiteit, die allemaal gerelateerd zijn aan de opstelling van elektronen.
Samenvattend: De vergelijkbare eigenschappen van elementen in dezelfde groep zijn uiteindelijk te wijten aan het feit dat ze hetzelfde aantal valentie -elektronen delen. Deze overeenkomst in elektronenconfiguratie bepaalt hun reactiviteit, bindingsgedrag en algemene chemische kenmerken.
 Welk element heeft vergelijkbare chemische eigenschappen als stikstof?
Welk element heeft vergelijkbare chemische eigenschappen als stikstof?  Vastestofelektrolyt met lithium-iongeleidbaarheid vergelijkbaar met vloeibare elektrolyten
Vastestofelektrolyt met lithium-iongeleidbaarheid vergelijkbaar met vloeibare elektrolyten Hoe interageren neutronen met reactormaterialen?
Hoe interageren neutronen met reactormaterialen?  Chemici maken circulaire fluorescerende kleurstoffen voor biologische beeldvorming
Chemici maken circulaire fluorescerende kleurstoffen voor biologische beeldvorming Wat is het gewicht van 0,8834 mol zuurstofgas?
Wat is het gewicht van 0,8834 mol zuurstofgas?
 VK publiceert plannen om het vervoer tegen het midden van de eeuw koolstofarm te maken
VK publiceert plannen om het vervoer tegen het midden van de eeuw koolstofarm te maken Canadese provincie belooft strijd tegen pijpleiding voort te zetten
Canadese provincie belooft strijd tegen pijpleiding voort te zetten Europees Parlement stopt met plastic waterflessen
Europees Parlement stopt met plastic waterflessen Ontbossing vanuit een bomenperspectief op de TED-conferentie
Ontbossing vanuit een bomenperspectief op de TED-conferentie Het oog van de tropische cycloon Herolds opent verder op NASA-satellietbeelden
Het oog van de tropische cycloon Herolds opent verder op NASA-satellietbeelden
Hoofdlijnen
- Onderscheid maken tussen organische moleculen zoals piepschuim en plastic die levende materie kenmerken?
- Wat is het voordeel van het feit dat het DNA goed is ingepakt in de chromosomen?
- De oorsprong van genen voor het maken van bloemen
- Een enkel ei wordt een genoemd?
- Welke structuren in het blad bevatten alle belangrijke organen?
- Niet-dodelijke parasieten verminderen de hoeveelheid die hun wilde gastheren eten, wat leidt tot ecosysteemeffecten
- De voordelen van de bestrijding van doornenkroon op het Great Barrier Reef
- Uit onderzoek blijkt dat hondenhersenen zowel verwerken wat we zeggen als hoe we dat zeggen
- Onderzoek werpt licht op hoe zeedieren stress overleven
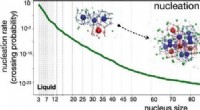
- Snelheidsvoorspelling voor homogene nucleatie van methaanhydraat
- Waarom sommige groenen bruin worden in historische schilderijen

- Groenere chemie door nieuwe benadering van katalyse

- Onderzoekslaboratoriumsimulator voltooit essentieel onderzoek naar geneesmiddelen in dagen

- Materiaalinformatica onthult nieuwe klasse van superharde legeringen

 Simulaties onthullen hydrodynamica van planetaire verzwelging door uitdijende ster
Simulaties onthullen hydrodynamica van planetaire verzwelging door uitdijende ster Wanneer Facebook, Twitter markeert berichten als niet-geverifieerd, lezers luisteren
Wanneer Facebook, Twitter markeert berichten als niet-geverifieerd, lezers luisteren Wat is de op een na moeilijkste natuurlijke substantie op aarde?
Wat is de op een na moeilijkste natuurlijke substantie op aarde?  Hoe testen wetenschappers ideeën over chemische evolutie?
Hoe testen wetenschappers ideeën over chemische evolutie?  Astronomen observeren het ontwaken van een Be/X-ray dubbelster
Astronomen observeren het ontwaken van een Be/X-ray dubbelster Een oceaan van sterrenstelsels wacht:nieuwe COMAP-radio-enquête
Een oceaan van sterrenstelsels wacht:nieuwe COMAP-radio-enquête  Wat beschrijft hoeveel energie er vrijkomt bij een aardbeving?
Wat beschrijft hoeveel energie er vrijkomt bij een aardbeving?  Onderzoekers demonstreren recordsnelheid met geavanceerde spectroscopietechniek
Onderzoekers demonstreren recordsnelheid met geavanceerde spectroscopietechniek
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

