
Wetenschap
Wat is de Lewis Dot -structuur van HC2H3O2?
1. Bepaal het centrale atoom:
* Koolstof is het meest waarschijnlijke centrale atoom in dit molecuul. Het heeft de capaciteit om vier bindingen te vormen, die nodig zijn om de andere atomen te verbinden.
2. Tel valentie -elektronen:
* h: 1 valentie -elektron elk (3 atomen =3 elektronen)
* C: 4 valentie -elektronen elk (2 atomen =8 elektronen)
* o: 6 valentie -elektronen elk (2 atomen =12 elektronen)
* Totaal: 3 + 8 + 12 =23 valentie -elektronen
3. Schik de atomen:
* De basisstructuur van azijnzuur is:
* H-C-C-O-H
* Het resterende zuurstofatoom zal binden aan de tweede koolstof.
4. Teken enkele bindingen:
* Sluit de atomen aan met enkele bindingen (één paar elektronen per binding).
* H-C-C-O-H
* o
5. Verdeel resterende elektronen:
* Vul de resterende valentie -elektronen rond de atomen in om een stabiel octet te bereiken (behalve voor waterstof, dat slechts 2 nodig heeft).
6. Vorm dubbele bindingen:
* Om octetten voor de koolstof- en zuurstofatomen te voltooien, moet u een dubbele binding vormen tussen de tweede koolstof en een van de zuurstofatomen.
Lewis puntstructuur van azijnzuur (HC₂H₃o₂):
`` `
O
||
H - C - C - O - H
|
H
`` `
belangrijke punten:
* De Lewis DOT -structuur vertegenwoordigt de meest waarschijnlijke opstelling van elektronen in het molecuul.
* De dubbele binding wordt meestal getrokken tussen het koolstof en het zuurstofatoom dat niet aan een waterstof wordt gebonden.
* De waterstofatomen worden vaak op een lineaire manier getekend voor duidelijkheid.
Laat het me weten als je wilt dat ik een van deze stappen in meer detail uitleg!
 Stel dat een ander onbekend zuur, sterke zuren, een diagram zijn om de deeltjes opgelost in water weer te geven en dit te beschrijven?
Stel dat een ander onbekend zuur, sterke zuren, een diagram zijn om de deeltjes opgelost in water weer te geven en dit te beschrijven?  Is stoffige lucht een element samengesteld homogeen mengsel of heterogeen mengsel?
Is stoffige lucht een element samengesteld homogeen mengsel of heterogeen mengsel?  De kern van een heliumatoom heet?
De kern van een heliumatoom heet?  Het maken van mRNA met een volledig chemisch proces kan aangepaste mRNA-vaccins mogelijk maken
Het maken van mRNA met een volledig chemisch proces kan aangepaste mRNA-vaccins mogelijk maken Welke moleculen vormen nuclieczuren?
Welke moleculen vormen nuclieczuren?
 Sommige slangen vertonen tekenen van zelfherkenning bij reuktests
Sommige slangen vertonen tekenen van zelfherkenning bij reuktests  Nieuwe studie van planktonschelpen vernietigt decennia-oud begrip van hun vorming en chemie
Nieuwe studie van planktonschelpen vernietigt decennia-oud begrip van hun vorming en chemie Klimaatverandering verandert de beschikbaarheid van terrestrisch water
Klimaatverandering verandert de beschikbaarheid van terrestrisch water Uitbreiding van de dode zone in de Arabische Zee verhoogt de angst voor klimaatverandering
Uitbreiding van de dode zone in de Arabische Zee verhoogt de angst voor klimaatverandering Machine-learningprogramma voorspelt gebruik openbaar vervoer in Singapore
Machine-learningprogramma voorspelt gebruik openbaar vervoer in Singapore
Hoofdlijnen
- Tot welk lichaamssysteem behoort het hoornvlies?
- Wat is een computersoftwareprogramma dat bestaat uit cellen met rijen en colums?
- Van baanbrekend tot baanbrekend:hoe een unieke tomatenmutatie de duurzame landbouw kan transformeren
- De wetenschapper die cellen gaf, was hun naam?
- Wat is 6000954 in wetenschappelijke notatie?
- Nieuw onderzoek laat zien hoe de malariaparasiet groeit en zich vermenigvuldigt
- Waarom hebben tong veel bacteriën?
- Welke microben zitten in je mond?
- Ontcijferen hoe licht de stomatale productie in planten regelt
- Ongebruikelijke kobaltverbinding ontwikkeld voor dunnefilmproductie

- Een nucleair ongeval met vermalen mineralen bevatten

- Wetenschappers werpen nieuw licht op moleculair gedrag

- Code voor fijnafstemming van elastomeren om biologische materialen na te bootsen
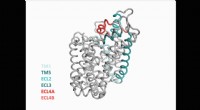
- Neurowetenschappers ontdekken nieuwe structuur van belangrijk eiwit in de hersenen
 Wat is de naam van de grond in een polaire toendra?
Wat is de naam van de grond in een polaire toendra?  Hoe NASA te helpen gegevens te verzamelen tijdens de aanstaande zonsverduistering
Hoe NASA te helpen gegevens te verzamelen tijdens de aanstaande zonsverduistering  Oceaanmonumenten worden geconfronteerd met mogelijk verlies van bescherming
Oceaanmonumenten worden geconfronteerd met mogelijk verlies van bescherming De hoeveelheid energie die de atmosfeer absorbeert, hangt af van het niveau van?
De hoeveelheid energie die de atmosfeer absorbeert, hangt af van het niveau van?  Zijn de lagen van de aarde het verst van de nieuwste en jongste lagen van korst?
Zijn de lagen van de aarde het verst van de nieuwste en jongste lagen van korst?  Uit onderzoek blijkt dat ouderlijke hulp bij huiswerk geen invloed heeft op de prestaties van leerlingen
Uit onderzoek blijkt dat ouderlijke hulp bij huiswerk geen invloed heeft op de prestaties van leerlingen Nieuw onderzoek onderzoekt hoe ziekten zich verspreiden bij primaten
Nieuw onderzoek onderzoekt hoe ziekten zich verspreiden bij primaten  Zwem kleine zwemmende robots zou op verre werelden naar leven kunnen zoeken
Zwem kleine zwemmende robots zou op verre werelden naar leven kunnen zoeken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

