
Wetenschap
Een metaal van wiens zouten zijn oplosbaar?
Dit is waarom:
* Oplosbaarheid is een complexe eigenschap: Oplosbaarheid hangt af van factoren zoals het type zout, het oplosmiddel (meestal water), temperatuur en de aanwezigheid van andere ionen.
* De meeste metalen vormen onoplosbare zouten: Zelfs zeer reactieve metalen zoals natrium en kalium vormen enkele onoplosbare zouten. Natrium vormt bijvoorbeeld een onoplosbaar zout met kalium hexanitrocobaltaat (III).
* Veel metalen vormen onoplosbare zouten met specifieke anionen: De meeste metalen vormen bijvoorbeeld onoplosbare zouten met sulfide -ionen (S²⁻).
Hoewel er geen metaal is met universeel oplosbare zouten, staan sommige metalen bekend om het vormen van zeer oplosbare zouten:
* Groep 1 metalen (alkali -metalen): Deze zijn over het algemeen zeer reactief en hun zouten zijn meestal erg oplosbaar.
* Groep 2 metalen (alkalische aardmetalen): Deze metalen vormen ook de neiging om oplosbare zouten te vormen, op enkele uitzonderingen.
Vergeet niet dat er altijd uitzonderingen en nuances in chemie zijn. Als u de oplosbaarheid van een specifiek zout moet bepalen, moet u naar een oplosbaarheidstabel verwijzen of een betrouwbare chemie -bron raadplegen.
 Gelaagde gassen dunne lucht weinig vocht zijn?
Gelaagde gassen dunne lucht weinig vocht zijn?  Cathinone-kleurtest is nu op de markt
Cathinone-kleurtest is nu op de markt Een stof verandert van een vaste stof in vloeistof?
Een stof verandert van een vaste stof in vloeistof?  Welk element is een kleurrijk reactief gas bij kamertemperatuur?
Welk element is een kleurrijk reactief gas bij kamertemperatuur?  Waarom kan calciumcarbonaat CACO4 electrisciteit uitvoeren wanneer gemengd met gedeïoniseerd water?
Waarom kan calciumcarbonaat CACO4 electrisciteit uitvoeren wanneer gemengd met gedeïoniseerd water?
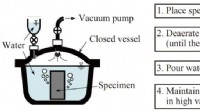
 Als de natuur een vacuüm verafschuwt, waarom zuigt het vacuüm van de ruimte dan niet de hele atmosfeer van de aarde weg?
Als de natuur een vacuüm verafschuwt, waarom zuigt het vacuüm van de ruimte dan niet de hele atmosfeer van de aarde weg?  Wetenschapsprojecten met Betta Fish
Wetenschapsprojecten met Betta Fish  Sterke aardbeving treft afgelegen berggebied in India
Sterke aardbeving treft afgelegen berggebied in India Experts vinden de oorsprong van Europa's klimaat verborgen in garnalenschelpen
Experts vinden de oorsprong van Europa's klimaat verborgen in garnalenschelpen Berekening van de ruwe geboortecijfer
Berekening van de ruwe geboortecijfer
Hoofdlijnen
- Welke factor is het minst waarschijnlijk bij te dragen aan een toename van de evolutiesnelheid?
- Nachtvliegers of dagjesmensen? Studie werpt licht op wanneer motten, vlinders zijn actief
- Is de wetenschap van het groeperen en noemen van organismen op basis van verschillen in overeenkomsten?
- Hoe de 'meesterregulatoren' van cellen DNA toegankelijk maken voor genexpressie
- Wat is een andere naam voor somatische stamcellen en wat doen ze?
- Met extra suiker, bladeren worden ook dik
- Is een kristal abiotisch of biotisch?
- Vaccinia-virus:nieuwe inzichten in de structuur en functie van het pokkenvirus-prototype
- Veel vis in de zee? Niet noodzakelijk, zoals de geschiedenis laat zien
- Gebruik maken van de slagvastheid van 's werelds hardste beton voor rampenpreventie
- Een nieuw begrip van eiwitbeweging
- Diep-UV-sonderingsmethode detecteert elektronenoverdracht in fotovoltaïsche energie

- Schimmel produceert zeer effectieve oppervlakteactieve stof

- De 3D-vorm van moleculen ontdekken met een druk op de knop
 Hoe geeft atomaire massa elementreactiviteit aan?
Hoe geeft atomaire massa elementreactiviteit aan?  Hoe de staart van de hagedis normaal intact kan blijven, maar kan afbreken wanneer dat nodig is
Hoe de staart van de hagedis normaal intact kan blijven, maar kan afbreken wanneer dat nodig is  Gas verandert rechtstreeks in een vaste stof Hoe beïnvloedt deze verandering de energie?
Gas verandert rechtstreeks in een vaste stof Hoe beïnvloedt deze verandering de energie?  Techbedrijf Slack maakt marktdebuut voor $26 referentieprijs
Techbedrijf Slack maakt marktdebuut voor $26 referentieprijs Röntgenmicroscoopoptiek lost 50 nm-kenmerken op en elimineert chromatische aberraties
Röntgenmicroscoopoptiek lost 50 nm-kenmerken op en elimineert chromatische aberraties Wanneer de muren van de Grand Canyon Sandstone lagen worden opgemaakt, snijdt een dijk in een paar wanneer gevormd?
Wanneer de muren van de Grand Canyon Sandstone lagen worden opgemaakt, snijdt een dijk in een paar wanneer gevormd?  Kunnen krassen gepolijst worden uit een saffierkristal?
Kunnen krassen gepolijst worden uit een saffierkristal?  Wetenschappers volgen patronen van eilandgroei in kristallen
Wetenschappers volgen patronen van eilandgroei in kristallen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

